ΚΑΡΚΙΝΟΣ ΠΡΟΣΤΑΤΟΥ
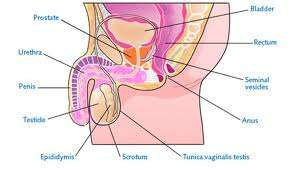
Ο καρκίνος του προστάτου είναι ο συχνότερος καρκίνος στους άνδρες στις Η.Π.Α. Παρ΄όλο το γεγονός ότι ο συγκεκριμένος καρκίνος μπορεί να διαγνωσθεί πρώιμα, υπολογίζεται ότι 335.000 νέες περιπτώσεις εμφανίστηκαν το 1998 εκ΄των οποίων οι 42.000 απεβίωσαν στις Η.Π.Α.
ΕΠΙΔΗΜΙΟΛΟΓΙΑ
Ηλικία: Ο κίνδυνος του να αναπτύξει κανείς καρκίνο προστάτου αρχίζει να αυξάνεται από την ηλικία των 50 ετών στους άνδρες της λευκής φυλής και οι οποίοι δεν έχουν οικογενειακό ιστορικό της νόσου και από την ηλικία των 40 ετών στους άνδρες της μαύρης φυλής και κυρίως σε αυτούς που έχουν ένα συγγενή Α΄ βαθμού (πατέρα ή αδελφό) με καρκίνο προστάτου. Φυλή: Η υψηλότερη επίπτωση καρκίνου προστάτου παγκοσμίως ανευρίσκεται σε άνδρες Αφρικανο-Αμερικανικής καταγωγής με ένα ρίσκο 9,8 % καθόλη την διάρκεια του βίου τους. Αυτός ο κίνδυνος είναι λίγο μεγαλύτερος από την επίπτωση το 8,0% που απαντάται στους λευκούς αμερικανούς.
ΑΙΤΙΟΛΟΓΙΑ ΚΑΙ ΠΑΡΑΓΟΝΤΕΣ ΚΙΝΔΥΝΟΥ
Ηλικία και Φυλή: Σειρές από νεκροτομικό υλικό δείχνουν ότι περίπου ένα ποσοστό 60% των ανδρών θα αναπτύξει καρκίνο προστάτου με την πάροδο της ηλικίας. Ο ισχυρότερος παράγοντας κινδύνου φαίνεται ότι είναι η ηλικία κυρίως στην μαύρη φυλή. Οικογενειακό Ιστορικό: Οι άνδρες που έχουν ένα συγγενή Α΄ βαθμού με καρκίνο προστάτου έχουν περίπου δύο φορές μεγαλύτερο κίνδυνο να αναπτύξουν καρκίνο προστάτου κατά την διάρκεια της ζωής τους, ενώ ο κίνδυνος γίνεται 9 φορές μεγαλύτερος σ΄αυτούς που έχουν δύο συγγενείς Α΄ βαθμού με καρκίνο προστάτου. Σεξουαλική δραστηριότητα/σεξουαλικά μεταδιδόμενα νοσήματα:
Δεν έχει βρεθεί συσχέτιση μεταξύ της σεξουαλικής δραστηριότητας ή των σεξουαλικά μεταδιδόμενων νοσημάτων και της επίπτωσης του καρκίνου προστάτου. Κληρονομικότητα: Ο κατ΄ εξοχήν κληρονομικός καρκίνος προστάτου εμφανίζεται σε μικρό αριθμό ανδρών ηλικίας < των 55 ετών. Το 88% των ανευπλοϊδικών όγκων του προστάτου έχουν βρεθεί στα χρωμοσώματα 7 ή και 8. Πρόσφατα οι Smith και συν αναφερόμενοι στο μοντέλο του αυτόσωμου επικρατούντος γονιδίου, το οποίο αναφέρθηκε και από τους Carter και συνεργάτες περιέγραψαν μία γενετική θέση στο χρωμόσωμα 1q 24-25 (1: HPC-1) με απόδειξη της σύνδεσης μετά από μια ανάλυση μιας ομάδας οικογενειών στη Βόρειο Αμερική και τη Σουηδία.
Πίνακας 1.
ΚΙΝΔΥΝΟΣ ΑΝΑΠΤΥΞΗΣ ΜΕΤΑΣΤΑΤΙΚΗΣ ΝΟΣΟΥ ΑΝΑΛΟΓΑ ΤΟ GLEASON SCORE ΣΕ ΑΣΘΕΝΕΙΣ ΜΕ ΚΑΡΚΙΝΟ ΠΡΟΣΤΑΤΟΥ
Gleason Score Κίνδυνος ανάπτυξης μεταστατικής νόσου (%)
2-4
5-7
8-10 20
40
75
ΠΑΘΟΛΟΓΟΑΝΑΤΟΜΙΚΗ ΤΑΞΙΝΟΜΗΣΗ
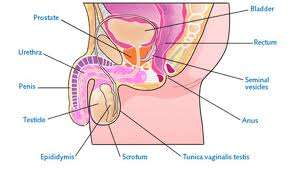
Αδενοκαρκίνωμα: Αποτελούν την πλειοψηφία του καρκίνου του προστάτου. Το 75% αναπτύσσεται στην περιφερική ζώνη, το 20% στην ενδιάμεση ζώνη και ένα 10% στην κεντρική ζώνη. Προγενές αδενοκαρκίνωμα (μπορεί να επεκτείνεται μέχρι την ουρήθρα). Βλεννώδες αδενοκαρκίνωμα (έκκριση μεγάλης ποσότητας βλέννης).
ΠΡΟΓΝΩΣΤΙΚΟΙ ΠΑΡΑΓΟΝΤΕΣ
Η επιβίωση είναι ανάλογη με την ηλικία του ασθενούς κατά την στιγμή της διάγνωσης, το στάδιο και το παθολογοανατομικό grading της νόσου. Γενικότερα ασθενείς με όγκους υψηλού βαθμού grading έχουν την τάση να υποτροπιάζουν γρηγορότερα και έχουν επιθετικότερη νόσο. Γενικά, μεταξύ των ανδρών που δεν έλαβαν θεραπεία η μέση επιβίωση κυμαίνεται στα 8-10 χρόνια σε αυτούς με στάδια Α ή Β, 3-6 χρόνια σε αυτούς με στάδιο C και 2-3 χρόνια σε αυτούς τους ασθενείς με στάδιο D.
ΘΕΡΑΠΕΙΑ
Θεραπεία τοπικής νόσου: Το Consensus Committee του Εθνικού Ιδρύματος Καρκίνου των Η.Π.Α. προτείνει: Η ριζική προστατεκτομή και η ακτινοθεραπεία είναι εξίσου αποτελεσματικές μέθοδοι θεραπείας για όγκους που εντοπίζονται στον προστάτη. Συγκριτικές μελέτες δείχνουν ισάξια ποσοστά 10ετούς επιβίωσης και με τις δύο θεραπευτικές μεθόδους. Ριζική προστατεκτομή: Παλαιότερα υπήρχε κίνδυνος θνητότητος με την ριζική προστατεκτομή. Μετά το 1980 οι κίνδυνοι από την αναισθησία, από τις απώλειες αίματος, από την μακροχρόνια παραμονή στο Νοσοκομείο έχουν ελαχιστοποιηθεί. Η σοβαρότερη επιπλοκή είναι η χρόνια ακράτεια και μόνο ένα 5% αυτών των ασθενών έχουν καλή ποιότητα ζωής.
Ακτινοθεραπεία
Εξωτερική ακτινοθεραπεία: Είναι η συνήθης μέθοδος ακτινοθεραπείας και ακτινοβολείται και η περιοχή των λεμφαδένων. Conformal εξωτερική ακτινοθεραπεία: Δημιουργεί τρισδιάστατη απεικόνιση των ακτινοβολουμένων Βραχυθεραπεία – Τοποθέτηση ραδιενεργών ισοτόπων: Τοποθετείται ραδιενεργό ισότοπο (iodine, paladium) παρουσίαζουν μικρότερο ρίσκο ακράτειας και θνητότητας συγκριτικά με την εξωτερική ακτινοθεραπεία. Τελευταία δοκιμάζονται μικτές τεχνικές, τοποθέτηση ενδοπροθέσεων σε συνδυασμό με εξωτερική ακτινοθεραπεία.
Θεραπεία τοπικής νόσου με αρνητικούς λεμφαδένες/ Συμπληρωματική θεραπεία
Ακτινοθεραπεία: Ασθενείς με παθολογοανατομική Τ3 νόσο μετά την ριζική προστατεκτομή είναι υποψήφιοι για συμπληρωματική θεραπεία. Αναμφίβολα η συμπληρωματική ακτινοθεραπεία ελαττώνει την τοπική υποτροπή. Ορμονοθεραπεία: Η συμπληρωματική ορμονοθεραπεία για την τοπικά προχωρημένη νόσο η οποία ακολουθεί την ριζική προστατεκτομή δεν έχει αποδεδειγμένο όφελος αλλά ακολουθείται από πολλούς ουρολόγους.
Ανδρογονικός αποκλεισμός και Ακτινοθεραπεία: Πλήρης ανδρογονικός αποκλεισμός μπορεί να επιτευχθεί με τους αγωνιστές LHRH μαζί με αντιανδρογόνα (φλουταμίδη). Η χρησιμοποίηση εγκαίρως του ανδρογονικού αποκλεισμού μπορεί να καθυστερήσει ή και ακόμα να προλάβει την ανάπτυξη μεταστατικής νόσου. Ανακουφιστική θεραπεία: Η ακτινοθεραπεία είναι πολύ αποτελεσματική στο να ελέγξει τον τοπικό πόνο που οφείλεται σε σκελετικές μεταστάσεις. Θεραπεία 30Gy σε 10 συνεδρίες ανακουφίζουν από τον πόνο και ελαττώνουν την χρήση αναλγητικών. Κρυοθεραπεία:
Με την βοήθεια διορθικού υπέρηχου διοχετεύεται υγρό άζωτο στον προστάτη. Αναφέρεται ελεύθερο νόσου διάστημα στην 2ετία σε ποσοστό 70%. Η μέθοδος είναι ακόμη υπό διερεύνηση.
ΟΡΜΟΝΟΘΕΡΑΠΕΙΑ
Χρησιμοποιείται για την τοπικά προχωρημένη νόσο καθώς επίσης ως προεγχειρητική, συμπληρωματική θεραπεία μαζί με ή όχι ακτινοθεραπεία. Ο ανδρογονικός αποκλεισμός επιτυγχάνεται είτε με αμφοτερόπλευρη ορχεκτομή, ή με ενέσεις αγωνιστών LHRH. Ο μέγιστος ανδρογονικός αποκλεισμός μπορεί να επιτευχθεί με πρόσθετη p. os χορήγηση αντιανδρογόνων (φλουταμίδη κ.α). Ο ενδιάμεσος ανδρογονικός αποκλεισμός είναι μια καινούργια προσέγγιση (θεραπεία για 2-3 μήνες ακολούθως διακοπή και επανέναρξη της θεραπείας ανάλογα της τιμής του PSA). Αμφοτερόπλευρη ορχεκτομή: Με αυτή την θεραπευτική προσέγγιση υπάρχει ελάττωση της τεστοστερόνης του πλάσματος σχεδόν 93%.
Η ψυχολογική επίπτωση της χειρουργικής στείρωσης είναι σοβαρή και πολλοί ασθενείς δεν την αποδέχονται και η φαρμακευτική θεραπεία είναι προτιμητέα. LHRH Aνάλογα: Leuprolide acetate (7.5 mg SC monthly) ή goserelin acetate (3.6 mg SC monthly) ρυθμίζουν την έκκριση της LH προκαλώντας χημική στείρωση.
Πλεονεκτούν στην αποφυγή του ψυχολογικού τραύματος της ορχεκτομής και ακόμη στις παρενέργειες από το καρδιαγγειακό σύστημα. Αντιανδρογόνα: Μπλοκάρουν τη δράση των ανδρογόνων στα επίπεδα του προστατικού αδένα, φαίνεται ότι δρουν σαν ενδιάμεσο στη σύνδεση του ενεργού μεταβολίτου της τεστοστερόνης της διυδροτεστοστερόνης με τον υποδοχέα της στο επίπεδο του προστατικού αδένα.
Τα συνήθη χρησιμοποιούμενα αντιανδρογόνα είναι androcur, flutamide, megestrol acetate. Αυτά προστίθενται στους αγωνιστές των LHRH για να μπλοκάρουν οποιοδήποτε ερεθισμό της τεστοστερόνης ή μπλοκάρουν απευθείας τα εναπομείναντα ανδρογόνα τα οποία μπορεί να επηρεάσουν τον προστάτη.
Συνδυασμένος ανδρογονικός αποκλεισμός: Η χειρουργική και φαρμακευτική στείρωση ελαττώνουν την κυκλοφορούσα τεστοστερόνη από 90-95%. Έχει δειχθεί ότι τα εναπομένοντα ανδρογόνα προέρχονται από τα επινεφρίδια. Πολλοί υποστηρίζουν ότι ο πλήρης ανδρογονικός αποκλεισμός επιτυγχάνεται προσθέτοντας φλουταμίδη. DES: Η χορήγηση διεθυλστιλβεστρόλης προκαλεί επίσης φαρμακευτική στείρωση.
Η DES αναστέλλει την ανάπτυξη του προστάτη πρωτοπαθώς μέσω αποκλεισμού της υποθαλαμοϋποφυσιακής οδού η οποία μπλοκάρει τη σύνθεση τεστοστερόνης από τους όρχεις και έχει ως αποτέλεσμα την ελάττωση της τεστοστερόνης στο πλάσμα.
ΘΕΡΑΠΕΥΤΙΚΕΣ ΣΥΣΤΑΣΕΙΣ
Ασθενής ο οποίος προσέρχεται με προχωρημένο καρκίνο προστάτου χρειάζεται χειρουργική ή φαρμακευτική στείρωση. Σε ασθενείς με μικρή συμμετοχή των οστών (κάτω από 5 οστικές περιοχές ο πλήρης ανδρογονικός αποκλεισμός είναι η θεραπεία εκλογής αυτό μπορεί να επιτευχθεί με ορχεκτομή ή με την χρήση ενέσεων leuprolide (7,5 mg SC monthly) περαιτέρω 90%ανδρογονικός αποκλεισμός επιτυγχάνεται με την προσθήκη φλουταμίδης 250 mg 2 φορές την ημέρα.
ΔΕΥΤΕΡΗΣ ΓΡΑΜΜΗΣ ΟΡΜΟΝΟΘΕΡΑΠΕΙΑ
Ακόμη και μετά την αποτυχία των αντι-ανδρογόνων μερικοί άρρωστοι θα οφεληθούν ξεκινώντας θεραπεία με αμινογλουτεθιμίδη κετοκοναζόλη ή γλυκοκορτικοειδή. Αναστολείς των επινεφριδιακών ανδρογόνων: Αμινογλοτεθιμίδη + υδροκορτιζόνη (RR : 49%-παρενέργειες, , πυρετός). Κετοκοναζόλη + υδροκορτιζόνη (RR : 80%-παρενέργειες, ακράτεια, επινεφριδιακή ανεπάρκεια, ηπατοτοξικότητα). Χημειοθεραπεία ορμονοανθεκτικής νόσου: Μετά την εγκατάσταση ορμονοαντοχής η μέση επιβίωση είναι 6-9 μήνες, η χημειοθεραπεία δεν έδειξε να οφελεί στην επιβίωση αλλά όμως βελτίωσε την ποιότητα ζωής αυτών των ασθενών.
Σουραμίνη: Σε μερικές μελέτες έδειξε ότι το 60% των ασθενών ελάττωσε τα επίπεδα του PSA πάνω από 50% και σε μερικές έδειξε όφελος στην επιβίωση. Εστραμουστίνη + πακλιταξέλη [RR 65%, παρενέργειες, λευκοπενία (38%), θρομβοπενία 13%, αναιμία 54%, καταβολή 33%]. Εστραμουστίνη + ντοσιταξέλη [RR 62% παρενέργειες, ουδετεροπενία 68%, θρομβοπενία 24%, υπασβεστιεμία 59%, τρανσαμινασεμία 47%]. Εστραμουστίνη + ετοποσίδη [RR 52%, πλεονεκτεί στην από το στόματος χορήγηση, παρενέργειες, αλωπεκία 100% λευκοπενία 57%, αναιμία 55% θρομβοπενία 56%]. Μιτοξαντρόνη + πρεδνιζόνη [RR 33% παρενέργειες καρδιοτοξικότητα (6%), ουδετεροπενία 45%, θρομβοπενία 5%, αλωπεκία 26%].
ΘΕΡΑΠΕΙΑ ΕΠΕΙΓΟΝΤΩΝ ΣΥΜΒΑΜΑΤΩΝ
Σε καθολικές οστικές μεταστάσεις η ημισωματική ακτινοβολία χρησιμοποιήθηκε καθώς επίσης και το ραδιενεργό στρόντιο (Metastron). Ανακούφιση από τον πόνο αναφέρθηκε στο 75% των περιπτώσεων μετά από διάστημα 3 εβδομάδων από την θεραπεία και μπορεί να συνεχιστεί για αρκετούς μήνες. Σαμάριο 153: Παρόμοιες ενδείξεις με το metastron με μικρότερη περίοδο ημιζωής. Διφοσφωνικά: Oυσίες οι οποίες αναστέλλουν την επαναπορόφηση των οστεοκλαστών στα οστά έδειξαν να έχουν ενθαρρυντικά αποτελέσματα στην αντιμετώπιση του πόνου και στη διατήρηση της οστικής μάζας.
Πίεση του νωτιαίου μυελού: Θεωρείται επείγον ογκολογικό σύμβαμα και δεν είναι ασύνηθες σε ασθενείς με μεταστατικό καρκίνο προστάτου και καθολικές οστικές μεταστάσεις και αυτό έγκειται σε μετάσταση στην σπονδυλική στήλη η οποία πιέζει το νωτιαίο μυελό.
Ασθενείς με υποψία σημείων πίεσης του νωτιαίου μυελού από την μαγνητική τομογραφία ή την αξονική μυελογραφία θα πρέπει να αντιμετωπίζονται με χορήγηση δεξαμεθαζόνης 4-6 mg ανά εξάωρο και ακολούθως θα πρέπει να υποβάλλονται σε ακτινοθεραπεία (30 Gy) σε 10 συνεδρίες στις προσβληθείσες περιοχές.
ΚΑΡΚΙΝΟΣ ΟΡΧΕΩΣ
Ο καρκίνος του όρχεως είναι σπάνιος (η συχνότητα εμφάνισης είναι <1% όλων των όγκων), αλλά αντιπροσωπεύει μία από τις συχνότερες κακοήθειες που εμφανίζονται στους νέους άνδρες. Θεραπεύεται σε μεγάλο ποσοστό και η διάρκεια της ζωής αυτών των ασθενών είναι πολύ μακρά. Απαιτείται μακροχρόνιο follow up στους θεραπευμένους ασθενείς.
ΚΛΙΝΙΚΕΣ ΕΚΔΗΛΩΣΕΙΣ
Επιδημιολογία: Για το 2000, 6.900 νέες περιπτώσεις και 300 θάνατοι εμφανίσθησαν στις ΗΠΑ. Αποτελεί το 1% όλων των κακοηθειών στους άνδρες. Η μεγαλύτερη συχνότητα εμφανίζεται μεταξύ της ηλικίας των 20 – 35 ετών. Παράγοντες κινδύνου: Η κρυψορχία (κυρίως όταν ο όρχις έχει παραμείνει στην κοιλιακή χώρα). Το σύνδρομο Klinefelter (ηυξημένος κίνδυνος εμφάνισης όγκων από γεννητικά κύττταρα στο μεσοθωράκιο).
ΔΙΑΓΝΩΣΗ
Οποιαδήποτε μάζα στους όρχεις στους άντρες θα πρέπει να εξετάζεται ώστε να αποκλειστεί η ύπαρξη καρκίνου όρχεως. Ο καρκίνος του όρχεως είναι ιάσιμος σε υψηλά ποσοστά (85% των περιπτώσεων). Η ιστολογική εξακρίβωση του τύπου του όγκου έχει προγνωστική και θεραπευτική σημασία. Διαγνωστική προσέγγιση: Σε εμφάνιση ογκιδίου στον όρχι, ο ασθενής υποβάλλεται σε αμφοτερόπλευρο υπερηχογράφημα όρχεων. Επί εμφάνισης καλοήθους όζου, ο ασθενής απλά παρακολουθείται. Επί ύπαρξης ύποπτης μάζας υποβάλλεται στις εξετάσεις: LDH, β-HCG, AFP και σε διαγνωστική ορχεκτομή. Επί εμφάνισης καλοήθειας απαιτείται απλή παρακολούθηση.
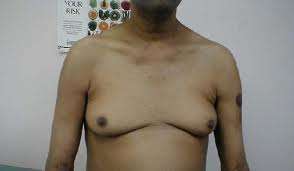
Εργαστηριακές Εξετάσεις
Serum α-fetoprotein (AFP): Ο βιολογικός χρόνος της ημισείας ζωής είναι περίπου 5 – 7 μέρες. Συνήθως, εκκρίνεται από τα καρκινικά κύτταρα εμβρυογενούς προέλευσης. Δεν εκκρίνεται από τα αμιγώς καθαρά σεμινώματα και η ανίχνευσή της καθορίζει την ύπαρξη μη σεμινωματώδους όγκου. Serum β-ΗCG: O χρόνος της ημισείας ζωής της είναι περίπου 24 ώρες. Μπορεί βιολογικά να είναι δραστήρια οδηγώντας σε αναστολή της παραγωγής οιστρογόνων από τους όρχεις και σε εμφάνιση γυναικομαστίας. Εκκρίνεται από τα συγκιοτροφοβλαστικά γιγαντοκύτταρα. Είναι παρούσα στα χοριοκαρκινώματα. Serum LDH: Χρησιμεύει σαν προγνωστικός δείκτης. Αντανακλά στον πολλαπλασιασμό ή στην σμίκρυνση του όγκου.
ΠΙΝΑΚΑΣ 1.
Όγκοι από γεννητικά κύτταρα και ιστοπαθολογικά χαρακτηριστικά τους
ΤΥΠΟΣ ΟΓΚΟΥ ΠΑΘΟΛΟΓΟΑΝΑΤΟΜΙΚΟ ΥΠΟΣΤΡΩΜΑ
Όγκοι από γεννητικά κύτταρα Σεμινώματα (40-50%)
Μονήρεις όγκοι (60%)
Μικτοί όγκοι (40%) Μη σεμινώματα (50-60%)
Όγκοι από εμβρυϊκά κύτταρα
Ογκοι Yolk sac
Τερατώματα
Χοριοκαρκινώματα
Όγκοι από γοναδικό στρώμα (1-2%) Κύτταρα Leydig
Κύτταρα Sertoil
Γοναδοβλάστωμα Γεννητικά κύτταρα + στρωματικά κύτταρα
Η PLAP (πλακουντιακή αλκαλική φωσφατάση) είναι θετική σε ενδιάμεσους όγκους αμφιβόλου ιστογένεσης. Αρνητική για χαμηλού μοριακού βάρους κερατίνες ανοσοιστοχημικά, εμφανίζονται στα σεμινώματα. Όγκοι οι οποίοι εκφράζουν χαμηλού μοριακού βάρους κερατίνες συνήθως είναι εμβρυϊκά καρκινώματα. Όγκοι από γεννητικά κύτταρα συνήθως είναι υπερπλοιδικοί. Η απώλεια του ετεροζυγώτη συχνά απεδείχθει σε πρώιμα στάδια της νόσου και δεν σχετίζεται με την πρόοδο της νόσου. 80% των περιπτώσεων έχουν ένα ισο-χρωμόσωμα στο βραχύ σκέλος του χρωμοσώματος 12[i(12p)], εμπλέκοντας ένα ή περισσότερα γονίδια στο 12p ή στην κακοήθη εξαλλαγή των γεννητικών κυττάρων.
ΠΡΟΓΝΩΣΗ
ΠΙΝΑΚΑΣ 2.
Διεθνής συναίνεση και κατηγοριοποίηση της πρόγνωσης των όγκων από γεννητικά κύτταρα
ΠΡΟΓΝΩΣΗ ΜΗ ΣΕΜΙΝΩΜΑΤΩΔΕΙΣ ΣΕΜΙΝΩΜΑΤΩΔΕΙΣ
Καλή Ύπαρξη όγκου στον όρχι ή
οπισθοπεριτοναϊκώς και μη ύπαρξη
πνευμονικών ή σπλαχνικών μεταστάσεων
AFP < 1.000 μg/mL
HCG < 5.000 IU/L
LDH < 1,5 των φυσιολογικών τιμών
Ύπαρξη όγκου σε οποιοδήποτε μέρος και μη ύπαρξη πνευμονικών ή σπλαχνικών μεταστάσεων
AFP < 1.000 μg/mL
Οποιαδήποτε τιμή HCG και LDH
Ενδιάμεση Ύπαρξη όγκου στον όρχι ή
οπισθοπεριτοναϊκώς και μη
ύπαρξη πνευμονικών ή σπλαχνικών
μεταστάσεων
AFP ? 1.000 μg/mL
HCG ? 5.000 IU/L
LDH ? 1,5 των φυσιολογικών τιμών
Ύπαρξη όγκου σε οποιοδήποτε μέρος και μη ύπαρξη πνευμονικών ή σπλαχνικών μεταστάσεων
AFP < 1.000 μg/mL
Οποιαδήποτε τιμή HCG και LDH
Κακή Ύπαρξη όγκου στο μεσοθωράκιο
πρωτοπαθώς και μη ύπαρξη
πνευμονικών ή σπλαχνικών μεταστάσεων
AFP > 10.000 μg/mL
HCG > 50.000 IU/L (10.000 μg/mL) ή
> 10 x από τα φυσιολογικά όρια
Κανείς άρρωστος δεν ταξινομείται ως κακής πρόγνωσης
ΘΕΡΑΠΕΙΑ
Θεραπευτική προσέγγιση αναφορικά με το στάδιο και τον ιστολογικό τύπο
AJCC Στάδιο Ι (Τ1-4, Ν0, Μ0, S0-3): Οι ασθενείς με σεμίνωμα υποβάλλονται σε ορχεκτομή και παρακολούθηση – follow up (κλινική αξιολόγηση, εργαστηριακός έλεγχος και αξονικές τομογραφίες) κάθε 2μηνο τον πρώτο χρόνο, κάθε 3μηνο τον δεύτερο χρόνο, κάθε 4μηνο τον τρίτο χρόνο, κάθε 6μηνο τον τέταρτο χρόνο και ακολούθως κάθε χρόνο. Σε ασθενείς με μη σεμίνωμα θετικούς λεμφαδένες και παθολογοανατομικό στάδιο ΙΙ θα λάβουν 2 κύκλους χημειοθεραπείας με το σχήμα BEP.
Αυτοί που έχουν αρνητικούς λεμφαδένες παθολογοανατομικού σταδίου Ι απαιτείται απλή παρακολούθηση κάθε 2μηνο τον πρώτο και δεύτερο χρόνο, κάθε 3μηνο τον τρίτο και τέταρτο χρόνο, κάθε 6μηνο τον πέμπτο χρόνο και ακολούθως κάθε χρόνο. AJCC Στάδια ΙΙ- ΙΙΙ (Τ1-4, Ν1-3, Μ0, S0-3) χωρίς μεταστάσεις: Σε ασθενείς με σεμίνωμα με φορτίο νόσου από την αξονική τομογραφία 5cm θα πάρουν 4 κύκλους EP ή 3 κύκλους BEP και ακολούθως απαιτείται παρακολούθηση κάθε 2μηνο τον πρώτο χρόνο, κάθε 3μηνο τον δεύτερο χρόνο, κάθε 4μηνο τον τρίτο χρόνο, κάθε 6μηνο τον τέταρτο χρόνο και ακολούθως κάθε χρόνο. Σε ασθενείς με μη σεμίνωμα, Αυτοί που έχουν >6 θετικούς λεμφαδένες ή θετικούς νεοπλασματικούς δείκτες θα πάρουν θεραπεία 4 κύκλους ΕΡ ή 3 κύκλους ΒΕΡ. Εάν μετά την θεραπεία δεν υπάρχει υπολειμματική νόσος και οι νεοπλασματικοί δείκτες είναι αρνητικοί απαιτείται παρακολούθηση ως ανωτέρω. Εάν οι νεοπλασματικοί δείκτες είναι θετικοί θα λάβουν επιπλέον 2 κύκλους ΒΕΡ. Σε αυτούς τους ασθενείς που μετά τους 3 πρώτους κύκλους ΒΕΡ έχουν ακόμη υπολειμματική νόσο απαιτείται χειρουργική αφαίρεση και εφόσον η ιστολογική δείξει κακοήθεια θα πάρουν άλλους 2 κύκλους ΒΕΡ. ΑJCC Στάδιο ΙΙΙ (Τ1-4, Ν1-3, Μ1, S0-3) με απομακρυσμένες μεταστάσεις: Όλοι αυτοί οι ασθενείς (με σεμίνωμα ή μη σεμίνωμα) θα υποστούν ορχεκτομή εφόσον είναι χαμηλού κινδύνου θα λάβουν 4 κύκλους ΕΡ ή 3 κύκλους ΒΕΡ.
Εάν είναι υψηλού κινδύνου θα λάβουν 4 κύκλους ΒΕΡ. Ακολούθως, εφόσον οι νεοπλασματικοί δείκτες είναι θετικοί μπορεί να αξιολογηθούν οι ασθενείς στο να λάβουν ακτινοθεραπεία (σεμινώματα) ή θεραπεία συντήρησης με 2 κύκλους ΒΕΡ ή θεραπεία διάσωσης με 4 κύκλους VIP. Επί αρνητικών νεοπλασματικών δεικτών εφόσον υπάρχει υπολειπόμενη νόσος οι ασθενείς χειρουργούνται και εφόσον υπάρχει κακοήθεια λαμβάνουν την ανωτέρω θεραπεία. Εάν δεν υπάρχει υπολειπόμενη νόσος ή το χειρουργείο δείξει καλοήθη μάζα τότε οι ασθενείς παρακολουθούνται, κλινικά και εργαστηριακά, κάθε 2μηνο τον πρώτο χρόνο, κάθε 3μήνο τον δεύτερο χρόνο, κάθε 4μηνο τον τρίτο χρόνο, κάθε 6μηνο τον τέταρτο χρόνο και ακολούθως κάθε χρόνο.
Πίνακας 3.
Συνήθη χρησιμοποιούμενα σχήματα
Σχήμα
EP Etoposide: 100 mg/m2/d x 5 μέρες
CDDP: 20 mg/m2/d x 5 μέρες
4 κύκλοι σε διάστημα 3 εβδομάδων
BEP Bleomycin: 30 U IV εβδομάδες d1, d9, d16
Etoposide: 100 mg/m2/d d1-d5
CDDP: 20 mg/m2/d d1-d5
2 – 4 κύκλοι σε διάστημα 3 εβδομάδων
VIP Vinblastine: 0,11 mg/kg εβδομάδα 1- 2
Ιfosfamide: 1,20 g/m2 IV/d d1-d5
Mesna: 400 mgr/m2 IV ανά 8ωρο d1-d5
CDDP: 20 mgr/m2 IV/d d1-d5
3 – 4 κύκλοι σε διάστημα 3 εβδομάδων
PVB CDDP: 20 mgr/m2 IV/d d1-d5
Vinblastine: 0,11 mg/kg ΙV/d d1-d5
Bleomycin: 30 U IV d2, d9, d16
3 κύκλοι σε διάστημα 3 εβδομάδων
Στο σεμίνωμα (για όλα τα στάδια), η θεραπευτική προσέγγιση έγγειται στο 90%. Όγκοι με μεικτά στοιχεία (σεμινωματώδη και μη) αντιμετωπίζονται ως μη σεμίνωμα. Σεμινώματα με υψηλή τιμή AFP αντιμετωπίζονται ως μη σεμίνωμα.
Ασθενείς με εγκεφαλικές μεταστάσεις πρέπει να λαμβάνουν ακτινοθεραπεία εγκεφάλου μαζί με χημειοθεραπεία. Μία μεγάλη τυχαιοποιημένη μελέτη έδειξε παρόμοια συνολική επιβίωση και ελεύθερο νόσου διάστημα για την χημειοθεραπεία με τα σχήματα BEP (bleomycin, etoposide, cisplatin) έναντι PVB (cisplatin, viblastine, bleomycin), και έναντι VIP (viblastine, ifosfamide, cisplatin). 4 κύκλοι BEP είναι ισοδύναμοι με 3 κύκλους BEP.
Τοξικότητα οφειλομένη στην χημειοθεραπεία
Στείρωση: Όλοι οι ασθενείς γίνονται ολιγοσπερμικοί κατά την θεραπεία και θα πρέπει να συστήνεται να φυλάσσουν το σπέρμα τους σε τράπεζα σπέρματος πριν την θεραπεία. Πνευμονική τοξικότητα: Σχετίζεται με την bleomycin, σπανίως θανατηφόρα σε συνολική αθροιστική δόση ? 400 μονάδων. Νεφροτοξικότητα: Μπορεί να εμφανιστεί σε σχήματα με βάση την πλατίνα. Νευροτοξικότητα και διαταραχές της ακοής: Σε σχήματα με βάση την πλατίνα. Καρδιαγγειακές επιπλοκές: Υπέρταση, φαινόμενο Raynaud, υπερχοληστεριναιμία. Δευτεροπαθείς κακοήθειες: Σε παρατεταμένη έκθεση σε αλκυλιούντες παράγοντες, ετοποσίδη, και στην χρήση ακτινοθεραπείας. Δευτεροπαθείς λευχαιμίες: Από την χρήση ετοποσίδης. Χαρακτηρίζεται από μετάθεση του χρωμοσώματος 11-q23 και συνήθως εμφανίζεται αρκετά χρόνια μετά την θεραπεία. Καρκίνοι στομάχου, ουροδόχου κύστεως και παγκρέατος: Σχετίζονται με έκθεση σε ακτινοβολία (σεμινωματώδεις όγκοι), περιορίζονται στο πεδίο της ακτινοθεραπείας και εμφανίζονται πολύ αργότερα μέσα σε μία δεκαετία και πλέον.
ΠΡΟΤΕΙΝΟΜΕΝΗ ΒΙΒΛΙΟΓΡΑΦΙΑ
1. Kenneth Pienta, Howard Sandler, Timothy Wilson et al.: In prostate cancer (chapter-19-in cancer management-a multidisciplinary approach). Edited by R. Pazdur, L. Coia, W. Hoskins, and L. Wagman, 1998, pp. 395 – 415.
2. Rogers E, Ohori M, Kaddabian VS, et al. Salvage radical prostatectomy: Outcome measured by serum prostate specific antigen levels. J Urol 153: 104, 1995. PSA levels after salvage radical prostatectomy.
3. Bubley GJ, Carducci M, Dahut W, et al. Eligibility and response guidelines for phase II clinical trials in androgen-independent prostate cancer: recommendations from the prostate-specific antigen working group. J Clin Oncol 1999; 17:3461 – 3467.
4. Oh WK, Kantoff PW: Management of hormone refractory prostate cancer: current standards and future prospects. J Urol 1998; 160:1220 – 1229.
5. Tannock I, Gospodarowicz M, Meakin W, et al. Treatment of metastatic prostatic cancer with low-dose prednisone: evaluation of pain and quality of life as pragmatic indices of response. J Clin Oncol 1989;7:590 – 597.
6. Petrylac DP, Macarthur RB, O’ Connor J, et al. Phase I trial of docetaxel with estramustine in androgen-independent prostate cancer. J Clin Oncol 1999; 17:958 – 967.
7. Pienta KJ, Redman B, Hussein M, et al.: Phase II evaluation of oral estramustine and oral etoposide in hormone-refactory adenocarcinoma of the prostate J Clin Oncol 1994; 12:2005.
8. Tannock IF, Osada D, Stockler MR, et al.: Chemotherapy with mitoxantrone plus prednisone or prednisone alone for symptomatic hormone-resistant prostate cancer: a Canadian randomized trial with palliative end points. J Clin Oncol 1996; 14:1756 , 1764.
9. Einhorn LH, Donohue JP. Advanced testicular cancer: update for urologists. J Urol 1998; 160: 1964 – 1969.
10. Travis LB, Curtis RE, Storm H, et al. Risk of second malignant neoplasms among long-term survivors of testicular cancer. J Natl Cancer Inst 1997; 89:1429 – 1439.
11. Einhorn LH. Testicular cancer: an oncological success story. Clin Cancer Res 1997; 3:2360 – 2632.