Τριπλά αρνητικός καρκίνος μαστού

Ο τριπλά αρνητικός καρκίνος μαστού (triple negative breast cancer, TNBC) χαρακτηρίζεται από την απουσία οιστρογονικών υποδοχέων (estrogen receptors, ER), υποδοχέων προγεστερόνης (progesterone receptors, PR) και έκφρασης του HER2/neu. Αν και ο TNBC δεν είναι η πλέον συχνή μορφή καρκίνου του μαστού στις γυναίκες (15-20%), χαρακτηρίζεται από φτωχή πρόγνωση, γεγονός που αποτελεί πρόκληση για τον κλινικό ογκολόγο, αφού ευθύνεται για δυσανάλογα πολλές περιπτώσεις μεταστατικής νόσου και θανάτου.1
TNBC, βασικού τύπου καρκίνωμα του μαστού και μεταλλάξεις του BRCA
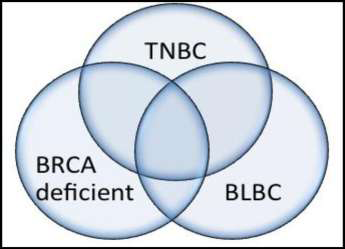
Ο όρος TNBC συσχετίζεται με το βασικού τύπου καρκίνωμα του μαστού (basal-like breast cancer, BLBC), αν και αποτελεί ξεχωριστή οντότητα από τον τελευταίο. Παράλληλα, πρόσφατες μελέτες έχουν αναδείξει συσχέτιση μεταξύ γυναικών με καρκίνο του μαστού που παρουσιάζουν μεταλλάξεις στο γονίδιο BRCA και του TNBC (Σχήμα 1). Το BRCA εμπλέκεται στους μηχανισμούς επισκευής του DNA, με αποτέλεσμα ασθενείς με μετάλλαξη στο γονίδιο να εμφανίζουν μεγαλύτερη προδιάθεση εμφάνισης καρκίνου. Η πλειοψηφία των TNBC εμφανίζεται σε γυναίκες με μεταλλάξεις στο BRCA και σε ποσοστό 80-90% γυναικών με BLBC.2
Σχήμα 1. Διάγραμμα που απεικονίζει την επικάλυψη μεταξύ του TNBC, του ΒLBC και των γυναικών με καρκίνο του μαστού που παρουσιάζουν μεταλλάξεις στο γονίδιο BRCA.
Χαρακτηριστικά των ασθενών και προγνωστική σημασία του TNBC
Γυναίκες με TNBC είναι πιο νέες σε ηλικία κατά την εκδήλωση της νόσου με τον TNBC να παρουσιάζεται ως καρκίνος πρώιμου σταδίου. Η νόσος είναι πιο συχνή σε προεμμηνοπαυσιακές Αφροαμερικανές γυναίκες. Ο BLBC χαρακτηρίζεται από ένα χαρακτηριστικό μοτίβο μετάστασης με προδιάθεση για μετάσταση περισσότερο στον εγκέφαλο και τους πνεύμονες και λιγότερο στα οστά, το ήπαρ και τους απομακρυσμένους λεμφαδένες. Ο TNBCs χαρακτηρίζεται από υψηλό πυρηνικό μιτωτικό δείκτη, μεγαλύτερο μέγεθος όγκου και από ένα πιο επιθετικό προφίλ γονιδιακής έκφρασης (χαμηλή έκφραση Bcl-2, υψηλή έκφραση p53 και Ki67).1
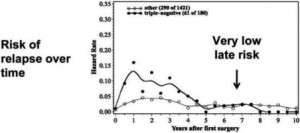
Ο TNBC χαρακτηρίζεται από μεγαλύτερη πιθανότητα υποτροπής (Σχήμα 2) και χειρότερη συνολική επιβίωση (overall survival, OS). Η πρόγνωση αυτή είναι ανεξάρτητη από άλλους παράγοντες όπως ο βαθμός του όγκου, το μέγεθός του και η λεμφαδενική διήθηση.2
Σχήμα 2. Διάγραμμα που απεικονίζει τον αυξημένο κίνδυνο υποτροπής στις γυναίκες με TNBC

Θεραπεία
O TNBC δεν είναι ευαίσθητος στη θεραπεία που χρησιμοποιείται σε όγκους του μαστού που υπερεκφράζουν τον HER2/neu (π.χ. μοριακή στόχευση με lapatinib και μονοκλωνικά αντισώματα όπως το trastuzumab) αλλά και στη θεραπεία που χρησιμοποιείται σε όγκους που είναι ER ± PR θετικοί (π.χ. εκλεκτικοί ρυθμιστές των υποδοχέων οιστρογόνων όπως το tamoxifen και το fulvestrant και αναστολείς αρωματάσης όπως η anastrazole και το exemestane). H συνδυασμένη κυτταροτοξική χημειοθεραπεία, χορηγούμενη σε συχνότερα χρονικά διαστήματα (μετρονομική χορήγηση), παραμένει η καλύτερη θεραπεία για τον TNBC αρχικού σταδίου.3
TNBC και προεγχειρητική/μετεγχειρητική (neoadjuvant/adjuvant) χημειοθεραπεία
Μελέτες σε ασθενείς με ΤΝBC οι οποίοι υποβλήθηκαν σε κυτταροτοξικές θεραπείας (συνδυασμοί με ανθρακυκλίνες ή ταξάνες) ανέδειξαν καλή ανταπόκριση του ασθενούς και υποχώρηση της νόσου στη χορήγηση πριν το χειρουργείο. Παρ’ όλα αυτά δεν αναδείχθηκε βελτίωση στην OS αφού παρατηρήθηκε υποτροπή της νόσου μέσα στην 5ετία. Εξάλλου, αναλύσεις πολλών μελετών με διάφορα χημειοθεραπευτικά σχήματα έχουν δείξει ότι είναι οι ασθενείς με TNBC που ωφελούνται περισσότερο από τη μετεγχειρητική θεραπεία.4-6
TNBC και στοχευμένες θεραπείες
Οι αναστολείς της πολυμεράσης της πολυαδενοφωσφορικής ριβόζης (polyADP-ribose polymerase, PARP) φαίνεται να αποτελούν το μέλλον στη θεραπεία των γυναικών με ΤNBC. Η PARP είναι μία πυρηνική πρωτεΐνη, η οποία είναι υπεύθυνη για την επισκευή βλαβών του DNA που επέρχονται φυσικά στα καρκινικά κύτταρα. Οι αναστολείς του ενζύμου PARP ενδέχεται να εμποδίζουν την επισκευή αυτή, ενισχύοντας με αυτόν τον τρόπο την αποτελεσματικότητα της χημειοθεραπείας. Οι κύριοι αναστολείς του PARP είναι η olaparib, η iniparib και η veliparib.2
Μελέτη φάσης Ι ανέδειξε ότι η οlaparib είχε δράση μόνο σε ασθενείς με μεταλλάξεις στο BRCA, ενώ μελέτη φάσης ΙΙ, σε ασθενείς με μετάλλαξη του BRCA, ανέδειξε ότι ασθενείς στους οποίους χορηγήθηκε olaparib σε υψηλότερη δόση (400mg δύο φορές ημερησίως) είχαν καλύτερη ανταπόκριση και ίδιο τοξικό προφίλ με ασθενείς χωρίς μετάλλαξη στο BRCA. H χορήγηση inaparib σε μία μελέτη φάσης II αύξησε την OS όταν χορηγήθηκε σε συνδυασμό με gemcitabine και carboplatin σε ασθενείς με TNBC.7-9
Πολλές μελέτες φάσεις Ι και ΙΙ βρίσκονται σε εξέλιξη στην προσπάθεια να επιλέξουμε τον κατάλληλο πληθυσμό ασθενών με TNBC οι οποίοι θα έχουν μεγαλύτερες πιθανότητες ανταπόκρισης στη στοχευμένη θεραπεία με αναστολείς PARP (Πίνακας 1).


Στοχευμένες θεραπείες για τον TNBC αποτελούν ουσίες που αναστέλλουν τον υποδοχέα του επιδερμικού αυξητικού παράγοντα (epidermal growth factor receptor, EGFR). Ο EGFR ενεργοποιεί την αντιγραφή του καρκινικού κυττάρου με τον ίδιο τρόπο όπως και ο HER2/neu. Στη στοχευμένη θεραπεία, η ενεργοποίηση αυτή μπορεί να μειωθεί με αποτέλεσμα την μείωση της ανάπτυξης του όγκου. Ο EGFR μπορεί να στοχευθεί με 2 τύπους ουσιών: τους αναστολείς της τυροσινικής κινάσης (tyrosine kinase inhibitors, TKIs), όπως η gefitinib και η lapatinib, και τα μονοκλωνικά αντισώματα (monoclonal antibodies, mAbs), όπως το cetuximab.2
Η συγχορήγηση gefitinib, docetaxel και carboplatin σε ασθενείς με TNBC αύξησε την ανταπόκριση στη θεραπεία, ενώ η gefitinib δεν ήταν αποτελεσματική ως μονοθεραπεία. Μελέτες για τη χορήγηση της lapatinib αναφέρουν απογοητευτικά αποτελέσματα εκτός από τις ασθενείς με όγκους του μαστού που εκφράζουν τον HER2.10-13
Μελέτες φάσεις II δεν έχουν αναδείξει όφελος από τη μονοθεραπεία με cetuximab σε ασθενείς με TNBC, αλλά έχουν αναδείξει όφελος στην αποτελεσματικότητα της μετεγχειρητικής χημειοθεραπείας. H προσθήκη cetuximab στο συνδυασμό carboplatin και irinotecan αύξησε την ανταπόκριση των ασθενών αλλά δεν βελτίωσε το ελεύθερο νόσου διάστημα (progression free survival, PFS). Άλλες μελέτες με mAbs δεν έχουν δώσει ενθαρρυντικά αποτελέσματα.14-15
Τέλος, αντιαγγειογεννετικές ουσίες, όπως η bevacizumab, έχουν δείξει αποτελεσματικότητα σε κάποιες γυναίκες με TNBC.16
Συμπέρασμα
Ο TNBC αποτελεί θεραπευτική πρόκληση, αφού η προσέγγισή του διαφέρει ως προς τη χημειοθεραπεία, την ορμονοθεραπεία και τη στοχευμένη θεραπεία. Απαιτούνται μεγαλύτερες και περισσότερες μελέτες που θα βοηθήσουν τον ογκολόγο να επιλέξει τον κατάλληλο πληθυσμό ασθενών με TNBC ο οποίος θα έχει μεγαλύτερες πιθανότητες ανταπόκρισης στις στοχευμένες θεραπείες.
ΒΙΒΛΙΟΓΡΑΦΙΑ
1. Santana-Davila R, Perez EA. Treatment options for patients with triple-negative breast cancer. J Hematol Oncol 2010;3:42.
2. Carey LA. Directed therapy of subtypes of triple-negative breast cancer. Oncologist 2010;15:49-56.
3. de Ruijter TC, Veeck J, de Hoon JP, van Engeland M, Tjan-Heijnen VC. Characteristics of triple-negative breast cancer. J Cancer Res Clin Oncol 2011;137:183-92.
4. Rouzier R, Perou CM, Symmans WF, et al. Breast cancer molecular subtypes respond differently to preoperativechemotherapy. Clin Cancer Res 2005;11:5678-85.
5. Carey LA, Dees EC, Sawyer L, et al. The triple negative paradox: primary tumor chemosensitivity of breast cancer subtypes. Clin Cancer Res 2007;13:2329-34.
6. Liedtke C, Mazouni C, Hess KR, et al. Response to neoadjuvant therapy and long-term survival in patients with triple-negative breast cancer. J Clin Oncol 2008;26:1275-81.
7. Fong PC, Boss DS, Yap TA, et al. Inhibition of poly(ADP-ribose) polymerase in tumors from BRCA mutation carriers. N Engl J Med 2009;361:123-34.
8. Tutt A, Robson M, Garber JE, et al. Oral poly(ADP-ribose) polymerase inhibitor olaparib in patients with BRCA1 or BRCA2 mutations and advanced breast cancer: a proof-of-concept trial. Lancet 2010;376:235-44.
9. O’Shaughnessy J, Osborne C, Pippen J, et al. Efficacy of BSI-201. A poly (ADP-ribose) polymerase (PARP1) inhibitor, in combination with gemcitamine/carboplatin in patients with metastatic triple negative breast cancer: results of a randomized phase II trial. J Clin Oncol 2008;26:abstr 1015.
10. Corkery B, Crown J, Clynes M, O’Donovan N. Epidermal growth factor receptor as a potential therapeutic target in triple negative breast cancer. Ann Oncol 2009;20:862-7.
11. Green MD, Francis PA, Gebski V, et al. Gefitinib treatment in hormone-resistant and hormone receptor-negative advanced breast cancer. Ann Oncol 2009;20:1813-17.
12. von Minckwitz G, Jonat W, Fasching P, et al. A multicentre phase II study on gefitinib in taxane- and anthracycline-pretreated metastatic breast cancer. Breast Cancer Res Treat 2005;89:165-72.
13. Burris HA III, Taylor CW, Jones SF, et al. A phase I and pharmacokinetic study of oral lapatinib administered once or twice daily in patients with solid malignancies. Clin Cancer Res 2009;15:6702-8.
14. Oliveras-Ferraros C, Vazquez-Martin A, Lopez-Bonet E, et al. Growth and molecular interactions of the anti-EGFR antibody cetuximab and the DNA cross-linking agent cisplatin in gefitinib-resistant MDA-MB-468 cells: new prospects in the treatment of triple negative/basal-like breast cancer. Int J Oncol 2008;33:1165-76.
15. Burness ML, Grushko TA, Olopade OI. Epidermal growth factor receptor in triple-negative and basal-like breast cancer: promising clinical target or only a marker? Cancer J 2010;16:23-32.
16. Miller K, Wang M, Gralow J et al. Paclitaxel plus bevacizumab versus paclitaxel alone for metastatic breast cancer. N Engl J Med 2007;357:2666-76.