Σχετικά με την μελέτη KEYNOTE-028 (Mesothelioma)
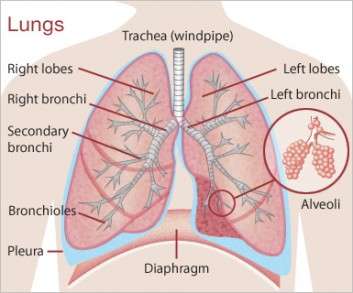
Η KEYNOTE-028 είναι μια εν εξελίξει, με πολλές ομάδες, μη τυχαιοποιημένη μελέτη Φάσης 1β, η οποία αξιολογεί την ασφάλεια, την ανεκτικότητα και την αντικαρκινική δράση του pembrolizumab σαν μονοθεραπεία (δοσολογία 10 mg/kg κάθε 2 εβδομάδες) σε 320 ασθενείς, με προχωρημένους συμπαγείς όγκους θετικούς στην έκφραση PD-L1, οι οποίοι είτε δεν ανταποκρίθηκαν στις υπάρχουσες θεραπείες είτε οι υπάρχουσες θεραπείες δεν είναι κατάλληλες.
Σχετικά με το κακοήθες μεσοθηλίωμα (Mesothelioma)
Τα κακοήθη μεσοθηλιώματα είναι καρκίνοι των υμένων που καλύπτουν τους πνεύμονες, την κοιλία, την καρδιά και τους όρχεις. Υπάρχουν τέσσερις κύριοι τύποι οι οποίοι χαρακτηρίζονται από την περιοχή που αναπτύσσονται: το θώρακα (υπεζωκοτικό μεσοθηλίωμα), την κοιλία (περιτοναϊκό μεσοθηλίωμα), την περιοχή κάλυψης γύρω από την καρδιά (περικαρδιακό μεσοθηλίωμα) και των υμένων που καλύπτουν τους όρχεις (μεσοθηλίωμα ελυτροειδούς χιτώνα όρχεων). Περίπου 3.000 νέα συμπτώματα μεσοθηλιωμάτων διαγιγνώσκονται κάθε χρόνο στις ΗΠΑ, με το 75% αυτών να αφορούν περιπτώσεις υπεζωκοτικού μεσοθηλιώματος. Η βασική αιτία για την εκδήλωση μεσοθηλιώματος είναι η έκθεση σε αμίαντο. Άλλοι παράγοντες κινδύνου μπορεί να είναι η μόλυνση με τον ιό των πιθήκων 40 (SV40), το γήρας (ηλικίες από 65 και πάνω) και το αρσενικό φύλο.
Τα αποτελέσματα της μελέτης KEYNOTE-006 πρώτης γραμμής για την αντιμετώπιση του προχωρημένου μελανώματος (Melanoma)
Η KEYNOTE-006 είναι μια παγκόσμια, ανοιχτή, τυχαιοποιημένη, πιλοτική μελέτη Φάσης 3, σε 834 ασθενείς από 16 χώρες, με ανεγχείρητο σταδίου ΙΙΙ προχωρημένο μελάνωμα και σταδίου IV, οι οποίοι δεν είχαν λάβει παραπάνω από μια συστηματική θεραπεία προηγουμένως. Οι δοσολογίες του pembrolizumab ήταν 10 mg/kg κάθε 2 εβδομάδες και 10 mg/kg κάθε 3 εβδομάδες σε σύγκριση με 4 κύκλους ipilimumab με δόση 3 mg/kg κάθε 3 εβδομάδες. Τα πρωτεύοντα καταληκτικά σημεία της μελέτης ήταν η Επιβίωση Χωρίς Εξέλιξη (PFS – Progression Free Survival) και η Συνολική Επιβίωση (OS – Overall Survival), ενώ τα δευτερεύοντα ήταν ο Συνολικός Δείκτης Ανταπόκρισης (ORR – Overall Response Rate), η διάρκεια της ανταπόκρισης και η ασφάλεια. Η ανταπόκριση του όγκου αξιολογείται στη 12η εβδομάδα και κατόπιν κάθε 6 εβδομάδες με ανεξάρτητη κεντρική επιθεώρηση βάσει των RECIST 1.1. Η πρώτη παρουσίαση των αποτελεσμάτων της KEYNOTE-006 βασίζεται σε ενδιάμεσες αναλύσεις που έγιναν για το δείκτη PFS με δεδομένα που ελήφθησαν μέχρι την 3η Σεπτεμβρίου 2014 (μέση παρακολούθηση 7,9 μήνες) και για τον δείκτη OS με δεδομένα που ελήφθησαν μέχρι την 3η Μαρτίου 2015 (μέση παρακολούθηση 13,8 μήνες).
Τα στοιχεία έδειξαν ότι το pembrolizumab ήταν ανώτερο του ipilimumab σε Επιβίωση Χωρίς Εξέλιξη – PFS, Συνολική Επιβίωση – OS και Συνολικό Δείκτη Απόκρισης – ORR (Melanoma)
Η διάμεση Επιβίωση Χωρίς Εξέλιξη – PFS του pembrolizumab ήταν 5,5 μήνες (ομάδα 2 εβδομάδων) και 4,1 μήνες (ομάδα 3 εβδομάδων), ενώ του ipilimumab ήταν 2,8 μήνες. Το εκτιμώμενο PFS στους 6 μήνες για το pembrolizumab και το ipilimumab ήταν 47,3%, 46,4% και 26,5%. Η Συνολική Επιβίωση – OS ενός έτους για το pembrolizumab ήταν 74,1% (ομάδα 2 εβδομάδων) και 68,4% (ομάδα 3 εβδομάδων), ενώ του ipilimumab ήταν 58,2%. Κατά το διάστημα διεξαγωγής της ανάλυσης, η διάμεση συνολική επιβίωση δεν εκπληρώθηκε από καμία ομάδα θεραπείας.
Ο Συνολικός Δείκτης Ανταπόκρισης ORR για το pembrolizumab ήταν 33,7% (ομάδα 2 εβδομάδων) και 32,9% (ομάδα 3 εβδομάδων) ενώ του ipilimumab ήταν 11,9%. Η Πλήρης Ανταπόκριση ήταν 5,0%, 6,1% και 1,4% αντίστοιχα. Οι ανταποκρίσεις ήταν εν εξελίξει σε ποσοστά 89,4% (ομάδα 2 εβδομάδων) και 96,7% (ομάδα 3 εβδομάδων) για ασθενείς που ελάμβαναν pembrolizumab και 87,9% για ασθενείς που ελάμβαναν ipilimumab. Η διάμεση ανταπόκριση δεν εκπληρώθηκε από την ομάδα 3 εβδομάδων του pembrolizumab και από το ipilimumab.
Τα προφίλ αποτελεσματικότητας και ασφάλειας ήταν παρόμοια στα 2 σχήματα pembrolizumab που αξιολογήθηκαν στη μελέτη. Δύο προηγούμενες μελέτες, η KEYNOTE-001 και η KEYNOTE-002, έδειξαν ότι η αποτελεσματικότητα και η ασφάλεια ήταν παρόμοια μεταξύ των δόσεων και των σχημάτων pembrolizumab που αξιολογήθηκαν; 10 mg/kg κάθε 2 εβδομάδες, 10 mg/kg κάθε 3 εβδομάδες και 2 mg/kg κάθε 3 εβδομάδες (η τρέχουσα εγκεκριμένη δοσολογία στις ΗΠΑ).
Αποτελέσματα ασφάλειας από την KEYNOTE-006 (Melanoma)
Το προφίλ ασφάλειας του pembrolizumab στη μελέτη ήταν γενικά συνεπές με τα όσα αναγράφονται στις πληροφορίες συνταγογράφησης. Οι πιο συχνά παρατηρούμενες ανεπιθύμητες ενέργειες οποιούδηποτε βαθμού που παρατηρήθηκαν στις ομάδες που έλαβαν το pembrolizumab, ήταν κόπωση, διάρροια, εξανθήματα και κνησμός. Για το ipilimumab, οι πιο συχνές ανεπιθύμητες ενέργειες σχετιζόμενες με τη θεραπεία ήταν κνησμός, διάρροια, κόπωση και εξανθήματα. Ανεπιθύμητες ενέργειες βαθμού 3 και 4 με pembrolizumab, παρατηρήθηκαν στο 13,3% των ασθενών της ομάδας 2 εβδομάδων και στο 10,1% της ομάδας των 3 εβδομάδων, ενώ για το ipilimumab το ποσοστό ήταν 19,9%. Η διακοπή της θεραπείας λόγω ανεπιθύμητων ενεργειών ήταν σπανιότερη με το pembrolizumab (ομάδες 2 και 3 εβδομάδων) απ’ ότι με το ipilimumab (4,0%, 6,9% και 9,4% αντίστοιχα). Ένας θάνατος στην ομάδα του ipilimumab αποδόθηκε στη θεραπεία της μελέτης.
Οι πιο συχνές ανεπιθύμητες ενέργειες αυτοάνοσης φύσεως ή σχετιζόμενες με το ανοσοποιητικό, που παρατηρήθηκαν κατά τη διάρκεια της θεραπείας με pembrolizumab (ομάδες 2 και 3 εβδομάδων) ήταν υποθυρεοϊδισμός (10,1% και 8,7%) και υπερθυρεοϊδισμός (6,5% και 3,2%). Με το ipilimumab αντίστοιχα παρατηρήθηκε κολίτιδα σε 8,2% των ασθενών. Ανεπιθύμητες ενέργειες βαθμού 3 και 4, φλεγμονώδεις ή σχετιζόμενες με το ανοσοποιητικό, που παρατηρήθηκαν σε περισσότερο από 1% των ασθενών που ελάμβαναν το pembrolizumab (ομάδες 2 και 3 εβδομάδων), ήταν κολίτιδα (1,4% και 2,5%) και ηπατίτιδα (1,1% και 1,8%), ενώ αντίστοιχα στο iplimumab ήταν κολίτιδα (7,0%) και υποφυσίτιδα (1,6%).
Σχετικά με το μελάνωμα (Melanoma)
Το μελάνωμα, η σοβαρότερη μορφή καρκίνου του δέρματος, χαρακτηρίζεται από ανεξέλεγκτη αύξηση των κυττάρων που παράγουν χρωστική ουσία. Η επίπτωση του μελανώματος παρουσιάζει αύξηση τις τελευταίες 4 δεκαετίες. Περίπου 232.130 νέα περιστατικά διαγνώστηκαν παγκοσμίως το 2012. Στις ΗΠΑ το μελάνωμα είναι ένας από τους συνηθέστερους τύπους καρκίνου που διαγιγνώσκονται και είναι υπεύθυνο για τη πλειονότητα των θανάτων από καρκίνο του δέρματος. Για το 2014 υπολογίζεται ότι θα διαγνωστούν περίπου 76.100 άνθρωποι με μελάνωμα, εκ των οποίων 9.710 αναμένεται να καταλήξουν από την ασθένεια αυτή, μόνο στις ΗΠΑ. Η επιβίωση στα πέντε έτη για το προχωρημένο ή το μεταστατικό μελάνωμα (Σταδίου IV) εκτιμάται σε 15 έως 20%.
Επιπρόσθετα ευρήματα της μελέτης KEYNOTE-001 για τον συνολικό υπό αξιολόγηση πληθυσμό (NSCLC)
Δεδομένα Επιβίωσης Χωρίς Εξέλιξη PFS και Συνολικής Επιβίωσης OS, βασισμένα σε έκφραση του PD-L1 στον όγκο, παρουσιάστηκαν επίσης από 356 πρωτοθεραπευόμενους ασθενείς καθώς και ασθενείς που είχαν λάβει προηγουμένως θεραπεία για τον προχωρημένο μη μικροκυτταρικό καρκίνο του πνεύμονα (συνολικό αξιολογήσιμο για χρώση PD-L1). Στην υπο-ομάδα ≥50% έκφρασης PD-L1, το μέσο PFS (95% CI) ήταν 6,3 μήνες (2,9 – 12,5) (n=119). Σε αυτή την υπο-ομάδα, το PFS ήταν 6,1 μήνες (2,1 – 12,5) για ασθενείς που είχαν λάβει θεραπεία προηγουμένως (n=294) και 12,5 μήνες (2,4 – 12,5) για πρωτοθεραπευόμενους ασθενείς (n=62). Το PFS ήταν 3,3 μήνες (95% CI, 2,1 – 4,1) για την υπο-ομάδα 1 – 49% έκφρασης PD-L1 (n=161) και 2,3 μήνες (95% CI, 2,1 – 4,0) για την υπο-ομάδα ≤ 1% έκφρασης PD-L1 (n=76). Η διάμεση OS δεν επετεύχθη στην υπο-ομάδα ≥ 50% έκφρασης PD-L1, ανεξαρτήτως προηγούμενης ή μη θεραπείας. Η διάμεση OS ήταν 8,8 μήνες για τις υπόλοιπες υπο-ομάδες (95% CI, 6,8 – 12,4 για την υπο-ομάδα 1-49% έκφρασης PD-L1 και 5,5 – 12 για την υπο-ομάδα ≤1% έκφρασης PD-L1, αντίστοιχα) και ήταν παρόμοια, ανεξαρτήτως προηγούμενης θεραπείας ή όχι.
Η διάμεση διάρκεια ανταπόκρισης ήταν παρόμοια έναντι διαφορετικών υπο-ομάδων έκφρασης PD-L1; 12,4 μήνες (2+ έως 22,8+) για την υπο-ομάδα ≥50% έκφρασης PD-L1, 10,3 μήνες (1,4+ έως 10,3+) για την υπο-ομάδα από 1 έως 49% έκφρασης PD-L1 και δεν επετεύχθη (0,9+ έως 10,8+) για την υπο-ομάδα ≤1% έκφρασης PD-L1. Κατά τη χρονική περίοδο της ανάλυσης, η διάμεση περίοδος παρακολούθησης ήταν 10,9 μήνες (εύρος, 5,2 – 27,5).
Οι ανεπιθύμητες ενέργειες που αξιολογήθηκαν στον συνολικό πληθυσμό της μελέτης, ήταν σύμφωνες με τα στοιχεία ασφαλείας που έχουν αναφερθεί προηγουμένως για το pembrolizumab. Οι συνήθεις ανεπιθύμητες ενέργειες ήταν κόπωση, κνησμός και μειωμένη όρεξη. Ανεπιθύμητες ενέργειες βαθμού 3 – 5 παρατηρήθηκαν σε 9,5% των ασθενών (n=47). Ανεπιθύμητες ενέργειες σχετιζόμενες με τη θεραπεία, αυτοάνοσης φύσεως ή σχετιζόμενης με το ανοσοποιητικό που παρατηρήθηκαν σε ποσοστό μεγαλύτερο του 2% ήταν αντιδράσεις σχετιζόμενες με την έγχυση (n=15; 3,0%), υποθυρεοϊδισμός (n=34; 6,9%) και πνευμονίτιδα (n=18; 3,6%). Ένα περιστατικό αντίδρασης στην έγχυση οδήγησε σε διακοπή της θεραπείας, ενώ όλα τα περιστατικά υποθυρεοϊδισμού αντιμετωπίστηκαν με τη κατάλληλη θεραπευτική αγωγή. Υπήρξε ένα θάνατος σχετιζόμενος με τη θεραπεία (πνευμονίτιδα), ενώ πνευμονίτιδα βαθμού 3 – 5 παρατηρήθηκε σε ποσοστό 1,8% των ασθενών (n=9). Κατά τη χρονική διάρκεια της ανάλυσης, δύο περιστατικά πνευμονίτιδας βρίσκονταν εν εξελίξει.
Σχετικά με την μελέτη KEYNOTE-001 και την αξιολόγηση του συνόλου δεδομένων για καρκίνους PD-L1 (NSCLC)
H ΚΕΥΝΟΤΕ-001 είναι μια εν εξελίξει, πολυκεντρική, ανοιχτή μελέτη Φάσης 1β ενός σκέλους, που αξιολογεί το pembrolizumab σε πάνω από 1.000 ασθενείς με ποικίλες μορφές κακοήθειας τελικού σταδίου – κυρίως καρκίνους του πνεύμονα και μελανώματα. Αξιολογήθηκαν τρία σχήματα δοσολογιών: 10 mg/kg κάθε 2 εβδομάδες, 10 mg/kg κάθε 3 εβδομάδες και 2 mg/kg κάθε 3 εβδομάδες. Τα πρωτεύοντα καταληκτικά σημεία περιλαμβάνουν τον Συνολικό Δείκτη Ανταπόκρισης – ORR και την ασφάλεια. Τα δευτερεύοντα καταληκτικά σημεία περιλαμβάνουν την Επιβίωση Χωρίς Εξέλιξη PFS, τη Συνολική Επιβίωση OS και τη διάρκεια ανταπόκρισης. Η ανταπόκριση του καρκίνου αξιολογείτο κάθε 9 εβδομάδες κατά RECIST 1.1 από ανεξάρτητες, κεντρικές, τυφλές ακτινογραφικές επιθεωρήσεις.
Σχετικά με τον καρκίνο του πνεύμονα (NSCLC)
Ο καρκίνος του πνεύμονα, που σχηματίζεται στους ιστούς των πνευμόνων, συνήθως σε κύτταρα που επικαλύπτουν τους αγωγούς αέρα, είναι η κυριότερη αιτία θανάτου από καρκίνο παγκοσμίως. Κάθε χρόνο πεθαίνουν περισσότεροι άνθρωποι από καρκίνο του πνεύμονα απ’ ότι από καρκίνο του παχέος εντέρου, του μαστού και του προστάτη μαζί. Οι δύο κύριες μορφές καρκίνου του πνεύμονα είναι ο μη μικροκυτταρικός καρκίνος (NSCLC) του πνεύμονα και ο μικροκυτταρικός καρκίνος του πνεύμονα (SCLC). Η μορφή NSCLC είναι η πιο κοινή μορφή καρκίνου του πνεύμονα, αποτελώντας περίπου το 85% των περιπτώσεων που διαγιγνώσκονται. Η επιβίωση 5 ετών για όλους τους προχωρημένους ή μεταστατικούς (Σταδίου IV) καρκίνους του πνεύμονα σε συνδυασμό, εκτιμάται σε 4%.
Σχετικά με τον PD-L1 και την έκφραση PD-L1 (NSCLC)
Ο PD-L1, γνωστός και ως προγραμματισμένος θάνατος – συνδέτης 1 (Programmed Death – Ligand 1), είναι μια πρωτεΐνη που απαντάται σε πολλούς τύπους κυττάρων, συμπεριλαμβανομένων και μερικών καρκινικών. Υπό φυσιολογικές συνθήκες, η αλληλεπίδραση του PD-L1 με μια άλλη πρωτεΐνη που ονομάζεται προγραμματισμένος θάνατος – υποδοχέας 1 (PD-1 – Programmed Death receptor – 1), χρησιμεύει σαν ένα σημαντικό σημείο ελέγχου του ανοσοποιητικού, το οποίο διατηρεί το ανοσοποιητικό σύστημα σε ισορροπία και εμποδίζει τον οργανισμό να «επιτεθεί» στα ίδια του τα κύτταρα όταν συμβαίνουν φλεγμονές ή μολύνσεις. Ωστόσο, όταν τα καρκινικά κύτταρα εκφράζουν τον PD-L1, διαφεύγουν του εντοπισμού και της καταστροφής τους από τα κυτταροτοξικά κύτταρα τύπου Τ – ένας τύπος ανοσοποιητικών κυττάρων – φονέων των καρκινικών – επιτρέποντας έτσι στον όγκο να επιζήσει και να αναπτυχθεί. Η έκφραση PD-L1 έχει παρατηρηθεί σε διάφορα επίπεδα σε πολλούς τύπους καρκίνου, συμπεριλαμβανομένων του καρκίνου του μαστού, του πνεύμονα και της κύστης. Μη φυσιολογικά υψηλά επίπεδα έκφρασης PD-L1, αποκαλούμενης υπερέκφρασης, είναι υπό εξέταση για τη πιθανότητα χρησιμοποίησής τους στην αναγνώριση ασθενών με αυξημένες πιθανότητες ανταπόκρισης σε συγκεκριμένες θεραπευτικές προσεγγίσεις βασισμένες στην ανοσολογία.