Νέα δεδομένα στη θεραπεία της χρόνιας αυτοάνοσης (ιδιοπαθής) θρομβοπενικής πορφύρας (ITP) μετά την έγκριση απο την ΕΕ της ελτρομβοπάγης.

Η Novartis έλαβε έγκριση στην ΕΕ για την ελτρομβοπάγη, ως πρώτο στην κατηγορία, θεραπευτικό παράγοντα για παιδιά ηλικίας άνω του ενός έτους με χρόνια αυτοάνοση (ιδιοπαθή) θρομβοπενική πορφύρα (ITP).
- Η έγκριση της ΕΕ για την ελτρομβοπάγη επεκτείνει τις θεραπευτικές επιλογές για τους παιδιατρικούς ασθενείς άνω του 1 έτους με χρόνια ITP που δεν έχουν ανταποκριθεί σε άλλες θεραπείες
- Δύο φαρμακοτεχνικές μορφές έχουν εγκριθεί: Δισκία για χορήγηση άπαξ ημερησίως και πόσιμο εναιώρημα σχεδιασμένο για μικρότερης ηλικίας παιδιά που ενδέχεται να μην μπορούν να καταπιούν δισκία
- Σχεδόν σε ένα στα τέσσερα παιδιά με ITP, η διαταραχή χαμηλού αριθμού αιμοπεταλίων και πιθανή αιμορραγία, μετατρέπεται σε χρόνια κατάσταση 1,2
Η Novartis ανακοίνωσε σήμερα ότι η Ευρωπαϊκή Επιτροπή έχει εγκρίνει την ελτρομβοπάγη για τη θεραπεία παιδιατρικών ασθενών (ηλικίας 1 έτους και άνω) με χρόνια αυτοάνοση (ιδιοπαθή) θρομβοπενική πορφύρα (ITP) που είναι ανθεκτικοί σε άλλες θεραπείες (π.χ. κορτικοστεροειδή, ανοσοσφαίρινες). Η έγκριση περιλαμβάνει τη φαρμακοτεχνική μορφή δισκίων καθώς και πόσιμου εναιωρήματος, που είναι σχεδιασμένο για νεότερους παιδιατρικούς ασθενείς που μπορεί να μην είναι ικανοί να καταπιούν δισκία. H ελτρομβοπάγη είχε εγκριθεί, από την Ευρωπαϊκή Επιτροπή, το 2010 για χρήση σε ενηλίκους με την ίδια πάθηση.
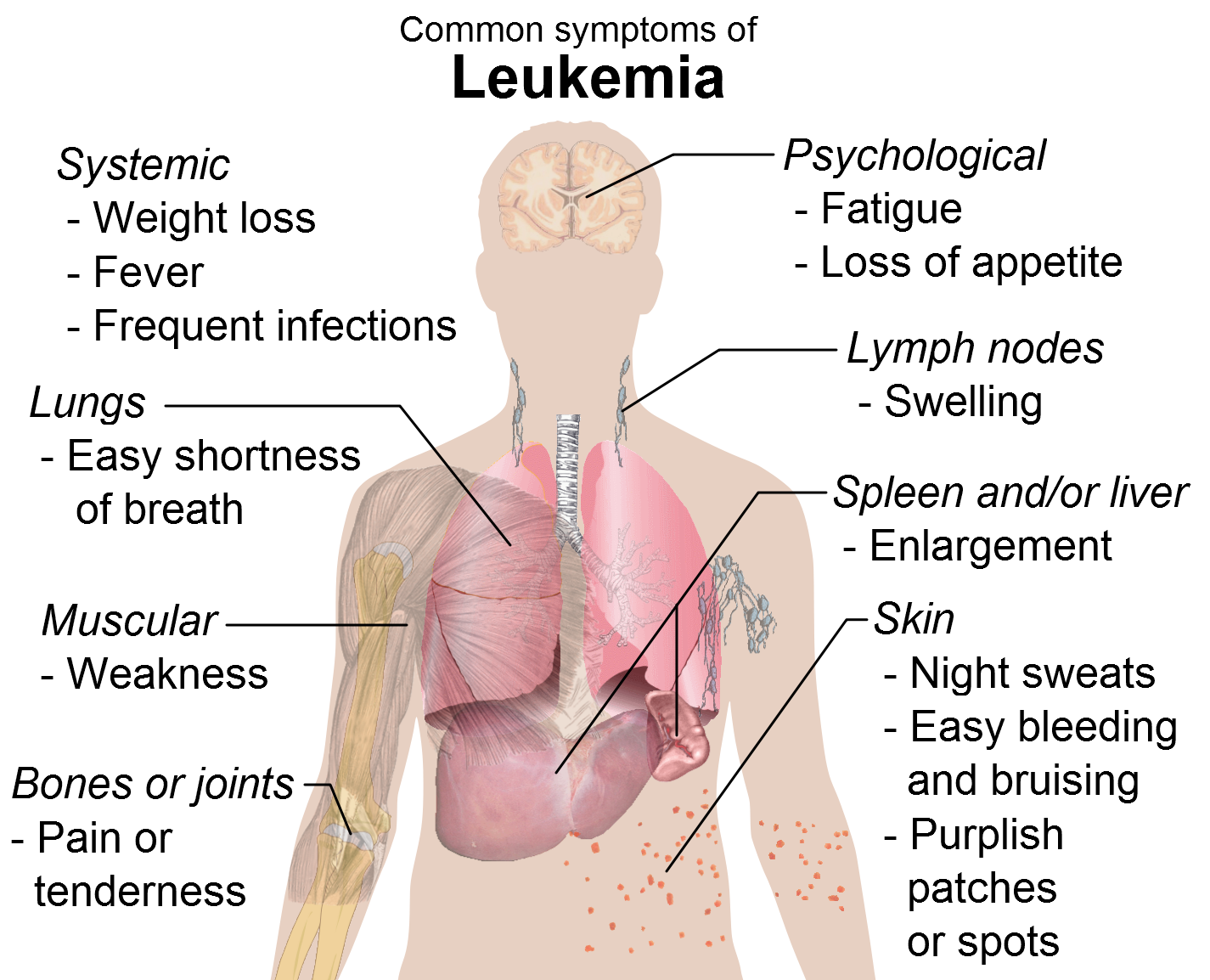
Η ITP είναι μια σπάνια αιματολογική διαταραχή που επηρεάζει σχεδόν πέντε ανά 100.000 παιδιά κάθε χρόνο και χαρακτηρίζεται από χαμηλό αριθμό αιμοπεταλίων2,3. Καθώς οι ασθενείς με ITP έχουν χαμηλό αριθμό αιμοπεταλίων, μπορεί να μελανιάζουν πιο εύκολα και να παρουσιάσουν αιμορραγία που είναι δύσκολο να σταματήσει2. Η χρόνια ITP, που ορίζεται ως εμμένουσα νόσος όταν διαρκεί για περισσότερο από 12 μήνες από τη διάγνωση4, παρατηρείται σε 13–36% των παιδιών με ITP1. Ένας μικρός αριθμός παιδιατρικών ασθενών με χρόνια ITP μπορεί να βρίσκεται σε κίνδυνο σημαντικής αιμορραγίας5.
Η έγκριση βασίζεται σε δεδομένα από δύο διπλά τυφλές, τυχαιοποιημένες, ελεγχόμενες με εικονικό φάρμακο μελέτες, συμπεριλαμβανομένης της μεγαλύτερης Φάσης III κλινικής δοκιμής σε αυτό τον πληθυσμό ασθενών. Σε αυτές τις μελέτες, οι ασθενείς στα σκέλη μελέτης και ελέγχου επιτρεπόταν να χρησιμοποιήσουν κάποιες σταθερές θεραπείες συντήρησης για την ITP, σύμφωνα με τις τοπικές θεραπευτικές πρακτικές. Η θεραπεία με την ελτρομβοπάγη αύξησε σημαντικά και διατήρησε τα επίπεδα αιμοπεταλίων στους παιδιατρικούς ασθενείς με χρόνια ITP που ήταν ανθεκτικοί ή είχαν υποτροπιάσει σε προηγούμενες θεραπείες για τη χρόνια ITP. Επίσης, ορισμένοι ασθενείς που λάμβαναν συγχορηγούμενες θεραπείες για την ITP είχαν τη δυνατότητα να μειώσουν ή να διακόψουν τη χρήση αυτών των θεραπειών, κυρίως των κορτικοστεροειδών.
Η έγκριση της Eυρωπαϊκής Επιτροπής ισχύει για όλα τα 28 κράτη μέλη της ΕΕ, καθώς και για την Ισλανδία, τη Νορβηγία και το Λίχτενστάιν.
Η ελτρομβοπάγη είναι ένας άπαξ ημερησίως, από του στόματος αγωνιστής του υποδοχέα θρομβοποιητίνης (TPO) που δρα προκαλώντας την ενεργοποίηση και τη διαφοροποίηση των μεγακαρυοκυττάρων (μεγάλων κυττάρων, που βρίσκονται ειδικά στο μυελό των οστών) από πρόδρομα κύτταρα του μυελού των οστών ώστε να αυξηθεί η παραγωγή αιμοπεταλίων6. Τον Αύγουστο του 2015, ο Οργανισμός Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) ενέκρινε τη νέα μορφή ως πόσιμο εναιώρημα, που επέκτεινε τη χρήση της ελτρομβοπάγης, ώστε να περιλαμβάνει παιδιά 1 έτους και άνω με χρόνια ITP, οι οποίοι είχαν μη επαρκή ανταπόκριση σε κορτικοστεροειδή, ανοσοσφαιρίνες ή σπληνεκτομή.
Σχετικά με τις κλινικές δοκιμές PETIT και PETIT2
Η PETIT είναι μια Φάσης II, πολυκεντρική, τριών σταδίων μελέτη που διερευνούσε την αποτελεσματικότητα, την ασφάλεια και την ανοχή της ελτρομβοπάγης σε παιδιατρικούς ασθενείς (ηλικιών 1 έως 17 ετών) που είχαν λάβει προηγούμενη θεραπεία για χρόνια ITP. Η μελέτη περιελάμβανε ασθενείς που ζούσαν με ITP για έξι μήνες ή περισσότερο και είχαν αριθμό αιμοπεταλίων <30 Gi/L. Το πρώτο στάδιο ήταν μία ανοιχτής επισήμανσης μελέτη που διερευνούσε τη δοσολογία. Το δεύτερο στάδιο ήταν διπλά τυφλό και ελεγχόμενο με εικονικό φάρμακο, και το τρίτο στάδιο ήταν επέκταση ανοιχτής επισήμανσης. Οι ασθενείς στη μελέτη μπορούσαν να χρησιμοποιήσουν κάποιες σταθερές θεραπείες συντήρησης για την ITP, σύμφωνα με τις τοπικές θεραπευτικές πρακτικές. Το πρωτεύον καταληκτικό σημείο αποτελεσματικότητας, που ήταν το ποσοστό των συμμετεχόντων που πέτυχαν αριθμό αιμοπεταλίων >=50 Gi/L χωρίς θεραπεία διάσωσης τουλάχιστον μία φορά μεταξύ των εβδομάδων ένα και έξι, επετεύχθη από 62% και 32% των ασθενών στο σκέλος της ελτρομβοπάγης και του συγκριτικού σκέλους, αντίστοιχα (p=0,011). Οι αναλύσεις του δευτερεύοντος καταληκτικού σημείου αποτελεσματικότητας απέδειξε κλινικά σημαντικό όφελος ως προς τη μειωμένη ανάγκη για θεραπείες διάσωσης (13% των ασθενών υπό ελτρομβοπάγη συγκριτικά με 50% των ασθενών στο σκέλος ελέγχου). Οι ασθενείς λάμβαναν ελτρομβοπάγη για συνολικά έξι μήνες κατά τη διάρκεια της μελέτης6,7.
Η PETIT2 είναι μια Φάσης III, πολυκεντρική, δύο τμημάτων κλινική δοκιμή που διερευνούσε την αποτελεσματικότητα, την ασφάλεια και την ανοχή της ελτρομβοπάγης σε παιδιατρικούς ασθενείς (ηλικιών 1 έως 17 ετών) που είχαν λάβει προηγούμενη θεραπεία για χρόνια ITP. Η μελέτη περιελάμβανε ασθενείς που ζούσαν με χρόνια ΙΤΡ για 12 μήνες ή περισσότερο και οι οποίοι είχαν μετρήσεις αιμοπεταλίων <30 Gi/L. Το πρώτο στάδιο ήταν τυχαιοποιημένο, διπλά τυφλό και ελεγχόμενο με εικονικό φάρμακο, και το δεύτερο στάδιο ήταν επέκταση ανοιχτού σχεδιασμού. Οι ασθενείς στη μελέτη επιτρεπόταν να χρησιμοποιήσουν κάποιες σταθερές θεραπείες συντήρησης για την ITP, σύμφωνα με τις τοπικές θεραπευτικές πρακτικές. Το πρωτεύον καταληκτικό σημείο αποτελεσματικότητας, που ήταν το ποσοστό των συμμετεχόντων που πέτυχαν αριθμό αιμοπεταλίων >=50 Gi/L χωρίς θεραπεία διάσωσης για τουλάχιστον έξι από τις οχτώ εβδομάδες μεταξύ των εβδομάδων πέντε και 12 του πρώτου μέρους της μελέτης, το πέτυχε το 40% των ασθενών που έλαβαν ελτρομβοπάγη και το 3% των ασθενών στο σκέλος ελέγχου (p<0,001). Αυτό το αποτέλεσμα ήταν συνεπές για όλες τις ηλικιακές ομάδες. Οι αναλύσεις του δευτερεύοντος καταληκτικού σημείου αποτελεσματικότητας έδειξαν κλινικά σημαντικό όφελος ως προς τη μειωμένη ανάγκη για θεραπεία διάσωσης (19% των ασθενών υπό ελτρομβοπάγη συγκριτικά με 24% των ασθενών στο συγκριτικό σκέλος) κατά την τυχαιοποιημένη, διπλά τυφλή περίοδο. Οι ασθενείς είχαν τη δυνατότητα να μειώσουν ή να διακόψουν τη θεραπεία έναρξης για την ΙΤΡ μόνο κατά τη φάση ανοιχτής επισήμανσης της μελέτης. Στην ανοιχτή επισήμανσης περίοδο μόνο με ελτρομβοπάγη, 15 από τους 87 ασθενείς λάμβαναν συγχορηγούμενες θεραπείες για την ITP κατά την έναρξη. Από αυτούς τους 15 ασθενείς, οχτώ (53%) είχαν παρατεταμένη μείωση ή μόνιμη διακοπή τουλάχιστον μιας θεραπείας ΙΤΡ που λάμβαναν κατά την έναρξη (επτά ασθενείς διέκοψαν οριστικά και ένας ασθενής είχε παρατεταμένη μείωση για >=18 εβδομάδες). Οι ασθενείς λάμβαναν ελτρομβοπάγη για συνολικά εννέα μήνες κατά τη μελέτη6,8.
Και στις δύο μελέτες, η ασφάλεια του υπό μελέτη πληθυσμού ήταν σύμφωνη με το γνωστό προφίλ ασφάλειας της ελτρομβοπάγης σε ενήλικες με χρόνια ITP. Δεν εντοπίστηκαν καινούριες ανεπιθύμητες ενέργειες. Οι πιο συχνές ανεπιθύμητες ενέργειες σε παιδιατρικούς ασθενείς άνω του 1 έτους με χρόνια ITP (με ποσοστό μεγαλύτερο ή ίσο του 10% και μεγαλύτερο από το εικονικό φάρμακο) ήταν η λοίμωξη του ανώτερου αναπνευστικού και η ρινοφαρυγγίτιδα6,7,8.
Σχετικά με τη χρόνια ITP
Η ITP είναι μια αιματολογική διαταραχή που χαρακτηρίζεται από το γεγονός ότι το αίμα δεν πήζει όπως θα έπρεπε λόγω χαμηλού αριθμού αιμοπεταλίων. Οι ασθενείς που πάσχουν από ITP συχνά έχουν μωβ μελανιές ή πολύ μικρές κόκκινες ή μωβ κηλίδες στο δέρμα. Συχνά μπορεί να πάσχουν από ρινορραγίες, αιμορραγίες στα ούλα κατά τις οδοντιατρικές εργασίες, ή άλλες αιμορραγίες που είναι δύσκολο να σταματήσουν. Στις περισσότερες περιπτώσεις, η ΙΤΡ θεωρείται ότι προκαλείται από μια αυτοάνοση αντίδραση, όπου το ανοσοποιητικό σύστημα ενός ανθρώπου επιτίθεται και καταστρέφει τα αιμοπετάλιά του2.
Οι δύο τύποι της ITP είναι η οξεία (προσωρινή ή βραχυπρόθεσμη) και η χρόνια (μακράς διάρκειας). Η οξεία ITP εμφανίζεται κυρίως σε παιδιά, συχνά μετά από μια ιογενή λοίμωξη, και γενικά διαρκεί λιγότερο από έξι μήνες. Ο αριθμός των αιμοπεταλίων επανέρχεται στο φυσιολογικό μέσα σε έξι έως 12 μήνες και μπορεί να μην απαιτείται θεραπεία2. Η χρόνια ITP, που ορίζεται ως συνεχιζόμενη ασθένεια για περισσότερο από 12 μήνες μετά τη διάγνωση4, εμφανίζεται στο 13-36% των παιδιών με ITP1. Ένας μικρός αριθμός παιδιατρικών ασθενών με χρόνια ITP μπορεί να διατρέχει κίνδυνο σημαντικής αιμορραγίας5.
Ο στόχος της θεραπείας στη χρόνια ITP στα παιδιά είναι να διατηρηθεί ένας ασφαλής αριθμός αιμοπεταλίων που να μειώνει τον κίνδυνο αιμορραγίας2.
Σχετικά με την ελτρομβοπάγη
Η ελτρομβοπάγη ανήκει σε μια κατηγορία φαρμάκων που ονομάζονται αγωνιστές υποδοχέων της θρομβοποιητίνης. Χρησιμοποιείται για να βοηθήσει στην αύξηση του αριθμού των αιμοπεταλίων στο αίμα. Τα αιμοπετάλια είναι αιμοσφαίρια που βοηθάνε στη μείωση ή την πρόληψη αιμορραγίας 6.
Σχετικά με τη Novartis
Η Novartis παρέχει καινοτόμες λύσεις στις αναφυόμενες ανάγκες των ασθενών και των κοινωνιών. Με έδρα στη Βασιλεία της Ελβετίας, η Novartis διαθέτει ένα διευρυμένο χαρτοφυλάκιο που καλύπτει άριστα αυτές τις ανάγκες: καινοτόμα φαρμακευτικά σκευάσματα, οφθαλμολογική φροντίδα και οικονομικώς συμφέροντα γενόσημα φάρμακα.
Η Novartis είναι η μόνη εταιρεία που κατέχει ηγετικές θέσεις σε αυτούς τους τομείς. Το 2014 οι πωλήσεις του Ομίλου ανήλθαν στα 58 δισ. δολάρια, ενώ επενδύθηκαν περίπου 10 δισ. δολάρια σε δραστηριότητες Έρευνας και Ανάπτυξης. Οι εταιρείες του Ομίλου Novartis απασχολούν περίπου 120.000 εργαζομένους και τα προϊόντα τους διατίθενται σε περισσότερες από 180 χώρες του κόσμου.
Στην Ελλάδα, η Novartis (Hellas) Α.Ε.Β.Ε. δραστηριοποιείται στον τομέα των συνταγογραφούμενων φαρμακευτικών ιδιοσκευασμάτων. Τα κεντρικά γραφεία βρίσκονται στη Μεταμόρφωση Αττικής και απασχολεί περίπου 500 άτομα.
Βιβλιογραφία
- George JN, Woolf SH, Raskob GE. Idiopathic thrombocytopenic purpura: a practice guideline developed by explicit methods for the American Society of Hematology. Blood. 1996;88(1):3-40.
- Immune Thrombocytopenia. US National Institutes of Health website. http://www.nhlbi.nih.gov/book/export/html/4917. Accessed February 1, 2016.
- Fogarty PF, Segal JB. The epidemiology of immune thrombocytopenic purpura. Curr Opin Hematol. 2007;14(5):515-519.
- Rodeghiero F, Stasi R, Gernsheimer T, et al. Standardization of terminology, definitions and outcome criteria in immune thrombocytopenic purpura of adults and children: report from an international working group. Blood. 2009;113(11):2386-2393.
- Neunert C, Lim W, Crowther M, et al. The American Society of Hematology 2011 evidence-based practice guideline for immune thrombocytopenia. Blood. 2011;117(16):4190-4207.
- Revolade Summary of Product Characteristics.
- Bussel JB, Garcia de Miguel P, Despotovic JM, et al. Eltrombopag for the treatment of children with persistent and chronic immune thrombocytopenia (PETIT): a randomised, multicentre, placebo-controlled study. Lancet Haematol. 2015; published online July 29, 2015.
- Grainger JD, Locatelli F, Chotsampancharoen T, et al. Eltrombopag for children with chronic immune thrombocytopenia (PETIT2): a randomised, multicentre, placebo-controlled trial. Lancet. 2015; published online July 29, 2015.