Νεφρική Οστική Νόσος: ερωτήσεις και απαντήσεις

Η Χρόνια Νεφρική Νόσος (ΧΝΝ) είναι μια κατάσταση που χαρακτηρίζεται από προοδευτική απώλεια της νεφρικής λειτουργίας με την πάροδο του χρόνου. Η ΧΝΝ περιγράφει μία κλινική οντότητα που προκαλεί βλάβη στα νεφρά και επηρεάζει την γενικότερη κατάσταση του οργανισμού.
Εάν η ασθένεια των νεφρών επιδεινώνεται, τα απόβλητα συγκεντρώνονται σε υψηλά επίπεδα στο αίμα και κάνουν το άτομο να αισθάνεται άρρωστο προκαλώντας επιπλοκές, όπως υψηλή αρτηριακή πίεση, αναιμία (χαμηλός αριθμός ερυθρών αιμοσφαιρίων), κακή διατροφική υγεία, νευρική βλάβη και τέλος μία «συστηματική» βλάβη στα οστά και στα αγγεία, γνωστή τα τελευταία χρόνια ως «νεφρική οστική νόσος».
Τι είναι η Νεφρική Οστική Νόσος
Η Νεφρική Οστική Νόσος, γνωστή παλαιότερα και ως Νεφρική Οστεοδυστροφία ή Δευτεροπαθής Υπερπαραθυεοειδισμός, αφορά παθολογικές καταστάσεις του αίματος, των οστών, των μαλακών μορίων και των αγγείων (στην πιο μοντέρνα εκδοχή της νόσου), που προκαλούνται από τις διαταραχές του μεταβολισμού του ασβεστίου, του φωσφόρου σε ασθενείς που πάσχουν από ΧΝΝ. Η εξέλιξη είναι αργή και προοδευτική, οι κλινικές εκδηλώσεις παρουσιάζονται όψιμα, ενώ προηγούνται ιστολογικές και βιοχημικές διαταραχές. Συγκεκριμένα η ΧΝΝ επηρεάζει τα οστά αλλάζοντας την ισορροπία μεταξύ φωσφόρου και ασβεστίου:
Περίσσεια φωσφόρου στο σώμα απομακρύνεται από τους νεφρούς, αλλά σε κατάσταση ΧΝΝ τείνει να συσσωρεύεται στο αίμα, οδηγώντας σε απώλεια του ασβεστίου από τα οστά.
Τέσσερεις μικροί αδένες (παραθυρεοειδείς), που βρίσκεται στο λαιμό, ρυθμίζουν την ομοιόσταση ασβεστίου στο σώμα. Μπορούν να γίνουν υπερβολικά δραστήριοι και να οδηγήσουν σε περαιτέρω απώλεια ασβεστίου από τα οστά.
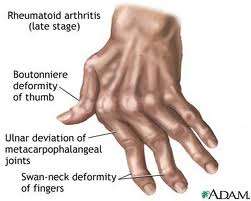
Oι κλινικές συνέπειες της παραπάνω κλινικής οντότητας είναι πόνοι στα οστά, κατάγματα, καρδιαγγειακά συμβάματα. Όλα τα παραπάνω συμβάματα οδηγούν αναπόφευκτα σε συχνές νοσηλείες και αυξημένη θνητότητα των ασθενών.
Ποιός είναι ο ρόλος της βιταμίνης D;
Η βιταμίνη D βελτιώνει την ομοιόσταση ασβεστίου σε ασθενείς με ΧΝΝ και μειώνει την υπερδραστηριότητα της παραθορμόνης (ΡΤΗ). Οι περισσότεροι άνθρωποι παίρνουν αρκετή βιταμίνη D μέσω συμπληρωμάτων διατροφής, και της έκθεσης στο ηλιακό φως. Αυτή η βιταμίνη D στη συνέχεια μετατρέπεται κανονικά από τα νεφρά σε μια «δραστική μορφή» η οποία μπορεί να χρησιμοποιηθεί από το σώμα. Σε ασθενείς με ΧΝΝ, η βιταμίνη D δεν μπορεί να μετατραπεί στην ενεργό μορφή, με αποτέλεσμα ο ασθενής να έχει έλλειμμα βιταμίνης D.
Η οξέωση που προκαλείται από την ΧΝΝ έχει σημασία;
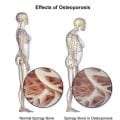
Το σώμα μας παράγει κανονικά οξύ, όταν διασπούνται ορισμένες πρωτεΐνες στη διατροφή μας ή κατά τη συνήθη διαδικασία της επισκευής και του κύκλου εργασιών των ιστών του σώματος. Αν κάποιος έχει οξέωση (πάρα πολύ οξύ), τα νεφρά του δεν είναι σε θέση να απαλλαγούν από την περίσσεια οξέος με την διούρηση. Η θεραπεία της οξέωσης προστατεύει τα οστά. Οστά τα οποία απελευθερώνουν ασβέστιο και φωσφόρο σε μία προσπάθεια να εξισορροπήσουν την περίσσεια οξέος, κατάσταση που οδηγεί σε οστεοπενία (μειωμένη πυκνότητα των οστών) και οστική νόσο σχετιζόμενη με την ΧΝΝ.
Η νεφρική οστική νόσος έχει σχέση με την καρδιαγγειακή νόσο;
Καρδιαγγειακή νόσος σημαίνει την ύπαρξη προβλημάτων με την καρδιά και τα αιμοφόρα αγγεία σε όλο το σώμα, συμπεριλαμβανομένου του εγκεφάλου, των πνευμόνων και των ποδιών.
Καρδιά και νόσος των αιμοφόρων αγγείων είναι συχνή σε άτομα με ΧΝΝ.
Με την πάροδο του χρόνου, τα αιμοφόρα αγγεία που μεταφέρουν το αίμα προς την καρδιά και τον εγκέφαλο μπορεί να αποφραχθούν από συσσώρευση κυττάρων, λίπους και χοληστερόλης.
Αυτό μειώνει τη ροή του αίματος προς την καρδιά και τον εγκέφαλο και μπορεί να προκαλέσει καρδιακές προσβολές και εγκεφαλικά επεισόδια. Οι ασθενείς με ΧΝΝ και σε αιμοκάθαρση έχουν αυξημένο κίνδυνο για καρδιαγγειακή νόσο. Αυτός ο αυξημένος κίνδυνος σχετίζεται με τη νεφρική νόσο και με άλλα προβλήματα υγείας, όπως ο διαβήτης και η υψηλή πίεση του αίματος.
Εκτός όμως από τους «παραδοσιακούς» παράγοντες κινδύνου η πρόληψη οφείλει να αφορά και τον μεταβολισμό των οστών. Το ασβέστιο και ο φώσφορος πρέπει να κρατιόνται σε ισορροπία σε ασθενείς με ΧΝΝ.
Και αυτό γιατί τα οστά χάνουν ασβέστιο και εξασθενίζουν με την πάροδο του χρόνου.
Κάποια ποσότητα ασβεστίου μπορεί να καταλήξει σε μέρη του σώματος, όπου δεν ανήκει, όπως την καρδιά και τα αιμοφόρα αγγεία. Αυτό κάνει τα αιμοφόρα αγγεία πιο σκληρά, λιγότερο ευένδοτα και με πιο στενό αυλό. Όταν συμβεί αυτό, θα είναι πιο πιθανό να έχουμε καρδιακή προσβολή ή εγκεφαλικό επεισόδιο. Η σύγχρονη βιβλιογραφία αναφέρει ότι εξαιτίας αυτού του μηχανισμού περίπου 80% των ασθενών με ΧΝΝ τελικού σταδίου παρουσιάζει ανιχνεύσιμες επασβεστώσεις στη στεφανιαία αρτηρία.
Οι αγγειακές επασβεστώσεις από μόνες τους αυξάνουν τον κίνδυνο καρδιαγγειακής θνητότητας σε ασθενείς με ΧΝΝ. Όλα τα δεδομένα υποστηρίζουν την ανάγκη για βέλτιστη αντιμετώπιση της νεφρικής οστικής νόσου και πρόληψη εμφάνισης προβλημάτων σαν τα παραπάνω.
Μπορεί επομένως για τη σωστή διαχείριση αυτής της κατάστασης να χρειαστεί να:
Ακολουθηθεί μια διατροφή που είναι χαμηλή σε υψηλής περιεκτικότητας σε φώσφορο τρόφιμα όπως τα ποτά τύπου cola, τα γαλακτοκομικά προϊόντα, τα ξερά φασόλια, τα μπιζέλια, τα καρύδια και οι σπόροι.
Να ληφθούν δεσμευτικά του φωσφόρου και/ή μια ενεργή μορφή της βιταμίνης D, που αναφέρεται να έχει και καρδιοπροστατευτικά χαρακτηριστικά μεταξύ των πλειοτρόπων δράσεων της.
Ο ρόλος της ρύθμισης του φωσφόρου
Ο φώσφορος είναι μία από τις πιο γνωστές τοξίνες, ενώ η υπερφωσφαταιμία συναντάται σε πάνω από το 50% παγκοσμίως στον αιμοκαθαιρόμενο πληθυσμό. Η απομάκρυνση φωσφόρου διαμέσου μίας συνεδρίας αιμοκάθαρσης σε ασθενή χωρίς υπολειπόμενη νεφρική λειτουργία είναι 20-40 mmol (κατά μέσο όρο 800 mg), που ισοδυναμεί εβδομαδιαίως με 60-120 mmol.
O διαιτητικός περιορισμός του φωσφόρου αποτελεί ακρογωνιαίο λίθο στην θεραπευτική στρατηγική. Υπολογίζεται ότι περίπου 1000 mg φωσφόρου την ημέρα προσλαμβάνονται διαμέσου των συντηρητικών και το 100% απορροφάται στην συστηματική κυκλοφορία, ποσοστό μεγαλύτερο από την απορρόφηση του φωσφόρου σε μη επεξεργασμένες τροφές.
Yπολογίζεται ότι περίπου 95% των ασθενών με ΧΝΝ υπό αιμοκάθαρση θα χρησιμοποιήσουν κάποια στιγμή κάποιας μορφής δεσμευτικά του φωσφόρου. Η χρήση των δεσμευτικών του φωσφόρου που περιέχουν ασβέστιο έχει μάλλον δυσμενή επίδραση στις αγγειακές επασβεστώσεις σε σύγκριση με πιο μοντέρνα δεσμευτικά φωσφόρου όπως η υδροχλωρική σεβελαμέρη.
Η σεβελαμέρη αντιπροσωπεύει ένα σημαντικότατο βήμα προόδου στη διαχείριση και αντιμετώπιση της υπερφωσφαταιμίας. Μιά άλλη μοντέρνα επιλογή δεσμευτικού του φωσφόρου είναι το λανθάνιο, μία ένωση ελεύθερη ασβεστίου και αλουμινίου, που έχει αποδειχτεί ότι διαθέτει φωσφοδεσμευτική δραστηριότητα παρόμοια με του αλουμινίου, με το πλεονέκτημα της ελάχιστης απορρόφησης.
Καλσιμιμιτικά
Τα καλσιμιμιτικά (calcimimetics) αποτελούν από μόνα τους μία κατηγορία φαρμάκων για τη θεραπεία του δευτεροπαθούς υπερπαραθυρεοειδισμού στοχεύοντας στην ριζική αντιμετώπιση του προβλήματος: O ανεπαρκής έλεγχος της PTH σχετίζεται με αυξημένο κίνδυνο θνητότητας.
Το cinacalcet είναι το πρώτο στην κατηγορία του που τροποποιεί τη δράση του υποδοχέα του ασβεστίου (calcium sensing receptor-CSR), αυξάνοντας την ευαισθησία του προς το εξωκυττάριο ασβέστιο. O CSR είναι ο κύριος ρυθμιστής της έκκρισης PTH και η ενεργοποίηση του διαμέσου των επιπέδων του ασβεστίου οδηγεί σε μία αλληλουχία ενδοκυτταρικών συμβάντων που προκαλούν μειωμένη έκκριση PTH. Ο ακριβής μηχανισμός δράση φαίνεται να σχετίζεται με την εξασθενημένη απελευθέρωση PTH και την επακόλουθη μετατροπή σε ανόργανες ουσίες των οστών, παρόμοια μ’ αυτήν που παρατηρείται κατά την περίοδο μετά τη χειρουργική παραθυρεοειδεκτομή (hungry bone syndrome).
Συμπέρασμα – Μελλοντικές κατευθύνσεις
Σημαντικές πρόοδοι στην κατανόηση των διαταραχών του οστικού μεταβολισμού στην ΧΝΝ έχουν γίνει τα τελευταία χρόνια. Ωστόσο, εξακολουθεί να υπάρχει ανάγκη για προοπτικές, τυχαιοποιημένες, ελεγχόμενες δοκιμές για την αξιολόγηση των αποτελεσμάτων του ελέγχου των επιπέδων φωσφόρου με τη χρήση συγκεκριμένων κλινικών κριτηρίων, όπως τη συχνότητα εμφάνισης καρδιαγγειακών συμβαμάτων. Μέχρι να φθάσουμε όμως σε αυτό το σημείο είναι ανάγκη να αξιοποιούνται όλα τα θεραπευτικά μέσα που έχουμε στη διάθεση μας σήμερα για τον έλεγχο του φωσφόρου, της παραθορμόνης με στόχο το καλύτερο κλινικό απότελεσμα ιδιαίτερα για το καρδιαγγειακό. Η νεφρική οστική νόσος είναι μια πολυπαραγοντική, ύπουλη, εξελικτική διαταραχή με σοβαρές συνέπειες για τον νεφροπαθή:
Ο ανεπαρκής έλεγχος των βιοχημικών παραμέτρων καθώς και η εξέλιξη των αγγειακών επασβεστώσεων αυξάνουν τον κίνδυνο καρδιαγγειακής νοσηρότητας και θνητότητας.
Η συμμόρφωση στην θεραπευτική αγωγή είναι βασικής σημασίας για την κλινική πορεία του ασθενούς, την αποφυγή καταγμάτων, καρδιαγγειακών συμβαμάτων και νοσηλειών, και τέλος την βελτίωση της ποιότητας της ζωής των ασθενών.
ΒΙΒΛΙΟΓΡΑΦΙΑ
1.Eriksen BO, Ingebretsen OC. The progression of chronic kidney disease: A 10-year population-based study of the effects of gender and age. Kidney Int 2006;69:375–82.
2. Tonelli M, Pfeffer MA. Kidney Disease and Cardiovascular Risk. Annu Rev Med 2007;58:123–39.
3. Chue CD, Townend JN, Steeds RP, Ferro CJ. Arterial stiffness in chronic kidney disease: causes and consequences. Heart 2010;96(11):817–23.
4. Menon V, Sarnak MJ. The epidemiology of chronic kidney disease stages 1 to 4 and cardiovascular disease: a high-risk combination. Am J Kidney Dis 2005; 45:223–32.
5. KDIGO: KDIGO Clinical Practice Guideline for the Diagnosis, Evaluation, Prevention, and Treatment of Chronic Kidney Disease-Mineral and Bone Disorder (CKD-MBD).
6. Black PS C, Scotland G, McCullough K, McGurn D, Robertson L, Fluck N, MacLeod A, McNamee P, Prescott G, Smith C, 1Section of Population Health UoA, Aberdeen, UK , 2Health Economics Research Unit UoA, Aberdeen, UK, 3NHS Grampian A, UK , 4Grampian University Hospitals NHS Trust A, UK: Early referral strategies for management of people with markers of renal disease: a systematic review of the evidence of clinical effectiveness, cost-effectiveness and economic analysis. Health technology assessment (Winchester, England). 2010;14(21):1–184.


Ιωάννης Γριβέας ,
Νεφρολόγος